题目内容
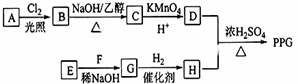
11.聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景.PPG的一种合成路线如图:
已知:①烃A的相对分子质量为70,
核磁共振氢谱显示只有一种化学环境的氢
②化合物B为单氯代烃:化合物C的分子式为C5H8
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质
④

回答下列问题:
(1)A的结构简式为
 .
.(2)由B生成C的化学方程式为
 .
.(3)由E和F生成G的反应类型为加成反应,G的化学名称为3-羟基丙醛.
(4)①由D和H生成PPG的化学方程式为

②若PPG平均相对分子质量为10000,则其平均聚合度约为b(填标号).
a.48 b.58 c.75 d.102
(5)D的同分异构体能同时满足下列条件的共有5种(不含立体异构);
①能与饱和NaHCO3溶液反应产生气体 ②既能发生银镜反应,又能发生皂化反应.
其中核磁共振请谱显示为3组峰,且峰面积比为6:1:1的是有
 (写结构简式)D的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是有有c(填标号).
(写结构简式)D的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是有有c(填标号).a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪.
分析 烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为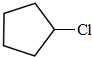 ,B发生消去反应生成C为
,B发生消去反应生成C为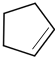 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(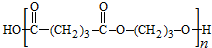 ),据此分析解答.
),据此分析解答.
解答 解:烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为 ,B发生消去反应生成C为
,B发生消去反应生成C为 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(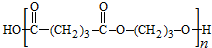 ),
),
(1)A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)由B生成C的化学方程式为 ,
,
故答案为: ;
;
(3)由E和F生成G的反应类型为加成反应,G的化学名称为3-羟基丙醛,故答案为:加成反应;3-羟基丙醛;
(4)①由D和H生成PPG的化学方程式为 ,
,
故答案为: ;
;
②若PPG平均相对分子质量为10000,则其平均聚合度约为$\frac{10000}{12×8+16×4+1×12}$≈58,故答案为:b;
(5)D的同分异构体中能同时满足①能与饱和NaHCO3溶液反应产生气体,含-COOH,②既能发生银镜反应,又能发生水解反应,D中共5个C,则含3个C-C-C上的2个H被-COOH、-OOCH取代,共为3+2=5种,含其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是 ,D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同,故答案为:5;
,D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同,故答案为:5; ;c.
;c.
点评 本题考查有机物推断,为高频考点,根据某些物质结构简式结合反应条件进行推断,注意题给信息的选取和正确运用,知道常见有机反应类型与其官能团的关系,题目难度不大.

| A. | Al2O3 $\stackrel{盐酸}{→}$AlCl3(aq)$\stackrel{蒸发}{→}$无水AlCl3 | |
| B. | Mg(OH)2$\stackrel{盐酸}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| C. | 粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | AgNO3(aq)$\stackrel{NH_{3}•H_{20}}{→}$Ag(NH3)2OH(aq)$→_{△}^{蔗糖}$Ag |
①亚硫酸钠溶液与稀盐酸 ②偏铝酸钠溶液与盐酸 ③二氧化碳与氢氧化钠溶液
④氯化铝与氨水 ⑤碳酸氢钠溶液与澄清石灰水
⑥碳酸氢钙溶液与澄清石灰水 ⑦苯酚钠溶液中通入二氧化碳.
| A. | 2组 | B. | 3组 | C. | 4组 | D. | 5组 |
| A. | 铝钠合金的熔点降低 | |
| B. | 铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na) | |
| C. | m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小 | |
| D. | 铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出 |
 碱金属元素的单质及其化合物被广泛应用于生产、生活中.
碱金属元素的单质及其化合物被广泛应用于生产、生活中.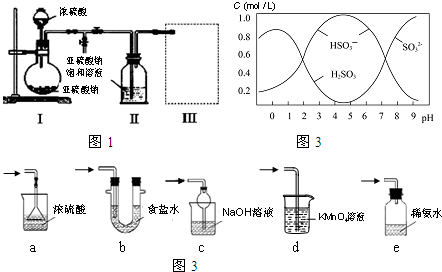

 .氧化剂为KClO3,浓盐酸的作用酸性、还原性.
.氧化剂为KClO3,浓盐酸的作用酸性、还原性.