题目内容
7.将金属钠投到装有水的烧杯中,并滴入2-3滴酚酞,观察到钠浮在水面上,说明钠的密度比水小,迅速融化成闪亮的小球,说明钠的熔点比较低,四处游动,发出“丝丝”的响声,溶液变为红颜色.分析 钠的密度小于水,熔点低,与水剧烈反应生成氢氧化钠和氢气同时放出大量热,现象总结为:浮水面、熔小球、乱游动、嘶嘶响,加入酚酞溶液变红.
解答 解:钠的密度比水小,熔点比较低,钠与水反应是放热反应,而且钠的熔点低,钠和水反应生成NaOH和氢气,生成的氢气使钠受力不均导致钠四处游动,H2燃烧时发出的咝咝声,钠与水反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,所以酚酞变红,故答案为:小;低;红.
点评 本题以钠和水反应为载体考查钠的性质,明确钠和水反应产生现象的原因,会根据实验现象,难点是化学用语的正确运用,为易错点.

练习册系列答案
相关题目
18.下列化学用语和描述均正确的是( )
| A. | 结构示意图为 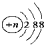 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 | |
| B. | 球棍模型为  的分子可发生加成反应 的分子可发生加成反应 | |
| C. | 邻硝基甲苯的结构简式为 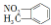 ,能发生取代反应 ,能发生取代反应 | |
| D. | 电子式分别为  和 和 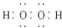 的两种化合物均为常见的氧化剂 的两种化合物均为常见的氧化剂 |
15.将Cl2和H2置于0.5L密闭容器中,反应20s后,生成2.0molHCl.在这段时间内,用HCl浓度变化表示的平均反应速率为( )
| A. | 20mol•(L•min)-1 | B. | 0.1mol•(L•s)-1 | C. | 0.2mol•(L•s)-1 | D. | 0.4mol•(L•min)-1 |
12.物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是( )
| A. | Na2CO3、NaHCO3、NaCl、NH4Cl | B. | Na2CO3、NaHCO3、NH4Cl、NaCl | ||
| C. | NH4Cl、(NH4)2SO4、Na2S、NaNO3 | D. | (NH4)2SO4、NH4Cl、NaNO3、Na2S |
8.下列离子方程式书写正确的是( )
| A. | 铜和稀硝酸反应 Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| B. | 碳酸氢钠和过量的澄清石灰水反应 2HCO3-+2OH-+Ca2+=CaCO3↓+2H2O+CO32- | |
| C. | Fe投入盐酸中 2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氢氧化铝溶于氢氧化钠溶液 Al(OH)3+OH-=AlO2-+2H2O |