题目内容
实验室制Cl2反应为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,则下列说法不正确的是( )
| ||
| A、还原剂是HCl,氧化剂是MnO2 |
| B、Cl2既是氧化产物又是还原产物 |
| C、每生成1molCl2转移电子的物质的量为2mol |
| D、每生成1molCl2有2molHCl被氧化 |
考点:氧化还原反应
专题:
分析:该反应中Mn元素化合价由+4价变为+2价、Cl元素化合价由-1价变为0价,得电子的化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,还原剂对应的产物是氧化产物,再结合物质间的反应分析解答.
解答:
解:A.反应中Cl元素化合价由-1价变为0价,被氧化,Mn元素化合价降低,被还原,则还原剂是HCl,氧化剂是MnO2,故A正确;
B.Cl元素化合价由-1价变为0价,被氧化,Cl2是氧化产物,故B错误;
C.Cl元素化合价由-1价变为0价,则每生成1molCl2转移电子的物质的量为2mol,故C正确;
D.由Cl元素化合价可知,生成1molCl2有2molHCl被氧化,故D正确.
故选B.
B.Cl元素化合价由-1价变为0价,被氧化,Cl2是氧化产物,故B错误;
C.Cl元素化合价由-1价变为0价,则每生成1molCl2转移电子的物质的量为2mol,故C正确;
D.由Cl元素化合价可知,生成1molCl2有2molHCl被氧化,故D正确.
故选B.
点评:本题考查了氧化还原反应,为高频考点,侧重于概念的理解,明确元素化合价及其变化是解本题关键,再结合基本概念来分析解答,题目难度不大.

练习册系列答案
相关题目
下列行为符合实验安全要求的是( )
| A、实验室废液可直接排入下水道 |
| B、制备有毒气体应在通风橱内进行 |
| C、配制稀硫酸时将水倒入浓硫酸中并不断搅拌 |
| D、不慎洒出的酒精在桌上着火时,立即用大量水扑灭 |
下列事实,不能用勒夏特列原理解释的是( )
| A、氯水中有下列平衡:Cl2+H2O?HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 |
| B、对2HI(g)?H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
| C、反应CO+NO2?CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
| D、合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施(N2+3H2?2NH3;△H<0) |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、标准状况下,4.0g CH4中含有共价键的数目为NA |
| B、常温常压下,6.4g氧气和臭氧中含有的分子总数为0.2NA |
| C、常温常压下,22.4LNH3约含有NA个NH3分子 |
| D、一定条件下6.4g SO2与足量氧气反应生成SO3,转移电子数为0.2NA |
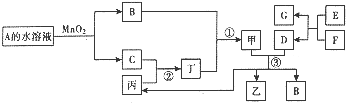 已知化合物A与B、丙与丁的组成元素相同,且四种物质中都含有同一种元素.A与B在常温下呈液态.D与F为常见金属单质,且D、F分别与甲的浓溶液分别在常温作用都无明显现象,加热时都有大量气体产生.E是一种红棕色粉末,A与丙可化合生成甲,乙、丙和B在常温下也可以生成甲和另一种化合物X,其部分转化关系如图(相关转化中部分反应条件和生成物未标出).
已知化合物A与B、丙与丁的组成元素相同,且四种物质中都含有同一种元素.A与B在常温下呈液态.D与F为常见金属单质,且D、F分别与甲的浓溶液分别在常温作用都无明显现象,加热时都有大量气体产生.E是一种红棕色粉末,A与丙可化合生成甲,乙、丙和B在常温下也可以生成甲和另一种化合物X,其部分转化关系如图(相关转化中部分反应条件和生成物未标出).