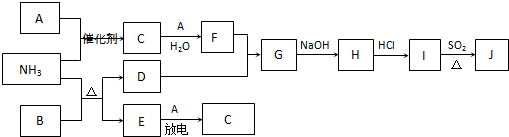
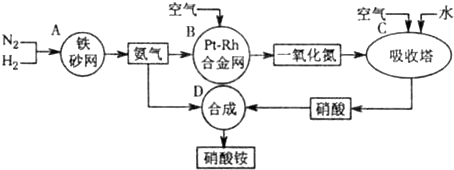
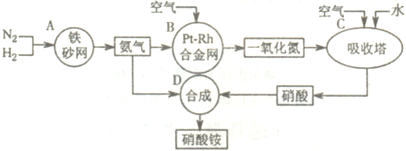
题目内容
31.已知:4NH3+5O2设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空及计算
(1)a mol NO完全转化为HNO3需要氧气_______ mol
(2)为使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为________(保留2位小数)。
(3)20.0 moL的NH3用空气氧化,产生混合物的组成为:NO 18.0 mol、O2 12.0 mol、N2 150.0 mol和一定量的硝酸,以及其它成分。(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率。
(4)20.0 moL 的NH3和一定量空气充分反应后,再转化为HNO3
①在下图中画出HNO3的物质的量n(A)和空气的物质的量n(B)关系的理论曲线。
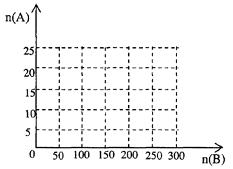
②写出当125≤n(B)≤200时,n(A)和n(B)的关系式______________________。
(1)0.75a
(2)0.14
(3)氨转化为NO和HNO3的转化率为97.5%
(4)①
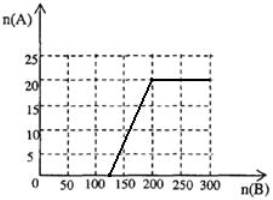
②3n(A)=0.8{n(B)-125}

练习册系列答案
相关题目
氮元素的单质和常见的化合物在工、农业生产中用途广泛.
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是 .
(2)雷雨时空气中的N2转化为NO,生成物NO是 色的气体, (填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应.NO2与水反应的化学方程式为 .
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为 ;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为 g.
(4)已知:4NH3+6NO
5N2+6H2O.化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).
①NH3与稀硫酸溶液反应的离子方程式为 ;
②为了比较不同催化剂的催化性能,需要测量并记录的数据是 .
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
| N2 | O2 | Ar | CO2 |
| -196℃ | -183℃ | -186℃ | -78℃ |
(2)雷雨时空气中的N2转化为NO,生成物NO是
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为
(4)已知:4NH3+6NO
| ||

若控制其他实验条件均相同,在催化反应器中装载不同的催化剂,将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液(溶液的体积、浓度均相同).
①NH3与稀硫酸溶液反应的离子方程式为
②为了比较不同催化剂的催化性能,需要测量并记录的数据是