题目内容
17.根据元素在周期表中的位置判断,下列元素中原子半径最小的是( )| A. | 钾 | B. | 镁 | C. | 硅 | D. | 氯 |
分析 钾在下一周期半径最大,镁、硅、氯同周期,随原子序数递增原子半径减小.
解答 解:钾在下一周期半径最大,镁、硅、氯同周期,随原子序数递增,原子核对核外电子吸引增大,原子半径减小,故原子半径:K>Mg>Si>Cl,故Cl原子半径最小,故选D.
点评 本题考查原子半径比较,比较基础,注意理解同周期、同主族元素性质递变性与相似性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.用NA表示阿伏加德罗常致,下列说法正确的是( )
| A. | 将lmol Cl2溶于水,所得溶液中HClO、Cl-和C1O-的总数目为2NA | |
| B. | 46g NO2和N2O4混合物中含分子数为NA | |
| C. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| D. | 适量Na2O2与CO2反应生成1mol O2时,转移的电子数为2NA |
12.在适当催化剂存在的条件下.对二甲苯(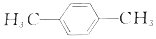 )与对苯二甲醛(
)与对苯二甲醛(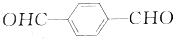 )均可被氧气直接氧化为对苯二甲酸,前后两种方案中,制备等量的对苯二甲酸时.理论上消耗的氧气物质的量之比为( )
)均可被氧气直接氧化为对苯二甲酸,前后两种方案中,制备等量的对苯二甲酸时.理论上消耗的氧气物质的量之比为( )
 )与对苯二甲醛(
)与对苯二甲醛( )均可被氧气直接氧化为对苯二甲酸,前后两种方案中,制备等量的对苯二甲酸时.理论上消耗的氧气物质的量之比为( )
)均可被氧气直接氧化为对苯二甲酸,前后两种方案中,制备等量的对苯二甲酸时.理论上消耗的氧气物质的量之比为( )| A. | 3:1 | B. | 2:1 | C. | 1:1 | D. | 4:1 |
2.微粒用${\;}_{Z}^{A}$Rn+表示,下列关于该微粒的叙述正确的是( )
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=A+Z |
9.下列图示与对应的叙述不相符的是( )
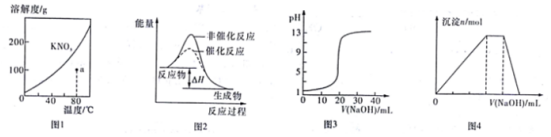

| A. | 图1表示KNO3的溶液曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 | |
| B. | 图2表示某放热反应分别有无催化剂的情况下反应过程中的能量变化 | |
| C. | 图3表示0.1000mol•L-1醋酸溶液得到的滴定曲线 | |
| D. | 图4表示向NH4Al(SO4)2溶液中逐滴滴加NaOH溶液,随着NaOH溶液体积V的变化,沉淀总物质的量n的变化 |
6.如图是实验室制取无水氯化镁的装置图,下列有关表述不正确的是( )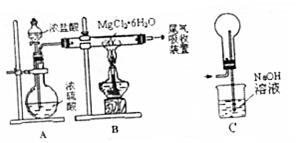

| A. | 装置A制取HCl利用了浓硫酸的吸水性 | |
| B. | 如果直接加热MgCl2•6H2O不能得到MgCl2,将得到Mg(OH)Cl或MgO | |
| C. | 用装置C做为尾气吸收装置,直接与B相连 | |
| D. | 这套装置在设计时未考虑反应结束后滞留在装置中的有害气体的吸收 |
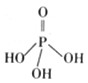 磷单质及其化合物的有广泛应用.
磷单质及其化合物的有广泛应用.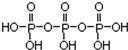 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10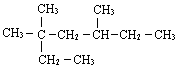 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷 2,3-二甲基1-丁烯
2,3-二甲基1-丁烯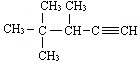 的系统名称为3,4,4-三甲基-1-戊炔
的系统名称为3,4,4-三甲基-1-戊炔 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷.