题目内容
(l)物质的量浓度相同的①氨水;②氯化铵;⑧碳酸氢铵;④硫酸氧铵;⑤硫酸铵5种溶液中c(NH4+)的大小顺序是 ,溶液pH的大小顺序是 .
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9..CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为 2×10-4mol?L-1,则生成沉淀所需CaCl2 溶液的最小浓度为
(3)己知:BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2mol-1
BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1
则反应 C(s)+CO2(g)═2CO(g)的△H3= kJ?mol-1.
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9..CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为 2×10-4mol?L-1,则生成沉淀所需CaCl2 溶液的最小浓度为
(3)己知:BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2mol-1
BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1
则反应 C(s)+CO2(g)═2CO(g)的△H3=
考点:离子浓度大小的比较,用盖斯定律进行有关反应热的计算
专题:
分析:(1)一水合氨是弱电解质,相同浓度的这几种溶液中铵根离子浓度最小,碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,根据离子水解程度结合化学式确定铵根离子浓度大小;
一水合氨是弱碱,溶液呈碱性,硫酸氢铵溶液为强酸性溶液,pH最小,再结合铵根离子水解程度确定溶液pH大小.;
(2)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=1×10-4mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍;
(3)依据热化学方程式和盖斯定律计算得到所需热化学方程式.
一水合氨是弱碱,溶液呈碱性,硫酸氢铵溶液为强酸性溶液,pH最小,再结合铵根离子水解程度确定溶液pH大小.;
(2)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=1×10-4mol/L,根据Ksp=c(CO32-)?c(Ca2+)计算沉淀时混合溶液中c(Ca2+),原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍;
(3)依据热化学方程式和盖斯定律计算得到所需热化学方程式.
解答:
解:(1)一水合氨是弱电解质,在水溶液里部分电离,所以相同浓度的这几种溶液中铵根离子浓度最小,硫酸铵中铵根离子个数是2,所以硫酸铵中铵根离子浓度最大,碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,所以氯化铵、碳酸氢铵、硫酸氢铵中铵根离子浓度大小顺序是④>②>③,则相同浓度的这几种溶液中c(NH4+)的由大到小顺序是⑤>④>②>③>①;
一水合氨是弱碱,溶液呈碱性,溶液碱性最强;硫酸氢铵溶液为强酸性溶液,pH最小,
碳酸氢根离子促进铵根离子水解,硫酸铵中铵根离子水解个数大于氯化铵,所以相同浓度的这几种溶液中
溶液pH的由大到小顺序是①>③>②>⑤>④,
故答案为:⑤>④>②>③>①;①>③>②>⑤>④;
(2)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=
×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,c(Ca2+)=
mol/L=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L,故答案为:5.6×10-5;
(3)己知:①BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2mol-1
②BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1
盖斯定律(①-②)×
得到,反应 C(s)+CO2(g)═2CO(g)的△H3=+172.5KJ/mol,
故答案为:+172.5.
一水合氨是弱碱,溶液呈碱性,溶液碱性最强;硫酸氢铵溶液为强酸性溶液,pH最小,
碳酸氢根离子促进铵根离子水解,硫酸铵中铵根离子水解个数大于氯化铵,所以相同浓度的这几种溶液中
溶液pH的由大到小顺序是①>③>②>⑤>④,
故答案为:⑤>④>②>③>①;①>③>②>⑤>④;
(2)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=
| 1 |
| 2 |
| 2.8×10-9 |
| 1×10-4 |
(3)己知:①BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2mol-1
②BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1
盖斯定律(①-②)×
| 1 |
| 2 |
故答案为:+172.5.
点评:本题考查了盐类水解,溶度积的有关计算、热化学方程式的书写,明确弱电解质的电离及盐类水解特点是解本题关键,难点是判断氯化铵和硫酸铵溶液pH大小,相同浓度的硫酸铵和氯化铵都是强酸弱碱盐,硫酸铵中铵根离子水解程度小于氯化铵,但硫酸铵中铵根离子水解个数大于氯化铵,为易错点,题目难度中等.

练习册系列答案
相关题目
下列有关溶液组成的描述合理的是( )
| A、无色溶液中可能大量存在Cu2+、NH4+、Cl-、S2- |
| B、中性溶液中可能大量存在Fe3+、K+、Cl-、CO32- |
| C、酸性溶液中可能大量存在Na+、ClO-、SO42-、I- |
| D、弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
将一定量的氯气通入50mL浓度为12.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是( )
| A、与NaOH反应的氯气一定为0.25 mol |
| B、n(Na+):n(Cl-)可能为7:3 |
| C、若反应中转移的电子为n mol,则0.30<n<0.45 |
| D、n(NaCl):n(NaClO):n(NaClO3)可能为11:1:2 |
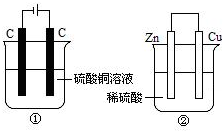 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A、产生气体体积 ①=② |
| B、①中阴极质量增加,②中正极质量减小 |
| C、溶液的pH变化:①减小,②增大 |
| D、电极反应式:①中阳极:4OH--4e-=2H2O+O2↑②中负极:2H++2e-=H2↑ |
用铂电极电解某溶液一段时间,该溶液浓度增大而pH减小,该溶液是( )
| A、NaOH |
| B、CuCl2 |
| C、CuSO4 |
| D、H2SO4 |
 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.已知充电时电池总反应为:LiMn2O4═Li1-xMn2O4+xLi,下列叙述正确的是( )
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.已知充电时电池总反应为:LiMn2O4═Li1-xMn2O4+xLi,下列叙述正确的是( )| A、放电时,正极反应为xLi++xe-═xLi |
| B、放电时,a极锂的化合价不发生变化 |
| C、充电时,b极发生氧化反应 |
| D、充电时,溶液中的Li+从b极向a极迁移 |
下列说法错误的是( )
| A、电解饱和食盐水可制取烧碱、氯气、氢气 |
| B、从海水中可提取镁、溴、碘等物质 |
| C、粗铜(含少量Zn、Fe、Pt等)电解精炼后,溶液中金属阳离子只有Fe2+、Zn2+ |
| D、在镀件上镀铜,镀件作阴极 |
 在容积为2.0L的密闭容器中,物质D在T℃时发生反应,某反应物和生成物的物质的量随时间t的变化关系如图.
在容积为2.0L的密闭容器中,物质D在T℃时发生反应,某反应物和生成物的物质的量随时间t的变化关系如图.