题目内容
6.有一不饱和的K0H溶液,加入xmolK2O或ymolK2O2或zmolK0H,均恰好得到同温度下的饱和K0H溶液,则x、y、z的关系正确的是( )| A. | z>y>x | B. | x=y>2z | C. | x=y<$\frac{z}{2}$ | D. | x=y>$\frac{z}{2}$ |
分析 根据K2O2与水反应进入水中的是K2O,与K2O与水反应一样,但两者都需要消耗水,而用KOH只需溶解在水中,不消耗水,故溶解的KOH多,根据K守恒来判断三者的关系.
解答 解:因K2O2与水反应进入水中的相当于是K2O,故K2O2与水的反应和K2O与水反应一样,两者都需要消耗水,根据K守恒,则有x=y;而用KOH只需溶解在水中,不消耗水,故需溶解的KOH的物质的量最多,根据K守恒,z>2y,即y<$\frac{z}{2}$,故选:C.
点评 本题若根据方程式来解答,比较繁琐,抓住反应的本质、K守恒能够快速解答.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
16.短周期元素X、Z、W、Q在元素周期表中的位置如图所示,其中X元素原子最外层电子数是最内层电子数的3倍,则下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | X、W能与钠形成摩尔质量相同的化合物 | |
| B. | 含X和Z元素的常见化合物为分子晶体 | |
| C. | 最高价氧化物对应的水化物酸性:W>Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |
17.下列物质在水溶液中没有漂白作用的是( )
| A. | Cl2 | B. | Na2O2 | C. | NaOH | D. | SO2 |
14.如图所示装置中电解质足量,阴离子交换膜(简称阴膜)只允许阴离子通过,下列有关说法正确的是( )
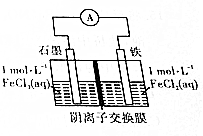

| A. | FeCl3和FeCl2可以互换位置,对反应无影响 | |
| B. | 该电池总反应为FeCl3+Fe═2FeCl2 | |
| C. | 若溶解2.8g铁,约有0.1molCl-从交换膜左向右迁移 | |
| D. | 一段时间后,阴膜左、右侧离子数变化量之比约为2:3 |
1.下述实验不能达到预期目的是:
| 编号 | 实验内容 | 实验目的 |
| A | 用平行光照射 | 区别淀粉溶液和氯化钠溶液 |
| B | 加入CaCO3粉末,充分反应后过滤 | 除去CaCl2溶液中的FeCl3 |
| C | 通过灼烧的Cu粉末,收集气体 | 除去N2中的少量O2 |
| D | 滴入稀盐酸,同时用pH计测定至溶液呈中性 | 除去KNO3溶液中的KOH |
11.室温下,0.1mol•L-1的盐酸滴定20.00mL0.1mol•L-1的某碱BOH溶液得到的滴定曲线如下,下列判断不正确的是( )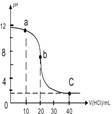

| A. | a点时,溶液呈碱性,溶液中c(B+)>c(Cl-) | |
| B. | b点时溶液的pH=7 | |
| C. | 当c(B+)=c(Cl-)时,v(HCl)<20mL | |
| D. | c点时溶液的c(H+)约为0.03mol•L-1 |
7.氯化铜的水溶液中存在下列可逆反应:下列方法能使蓝色的氯化铜溶液变成黄绿色的是( )
[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
淡蓝色 黄绿色.
[Cu(H2O)4]2++4Cl-?[CuCl4]2-+4H2O
淡蓝色 黄绿色.
| A. | 加蒸馏水 | B. | 加浓盐酸 | C. | 加AgNO3溶液 | D. | 加氢氧化钠溶液 |
4.碳酸氢钠是焙制糕点所用的发酵粉的主要成分之一.碳酸氢钠(NaHCO3)属于( )
| A. | 氧化物 | B. | 酸 | C. | 碱 | D. | 盐 |
5.下列实验操作中错误的是( )
| A. | 由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 使用容量瓶前检查它是否漏水 | |
| D. | 蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热 |