题目内容
下列有关分子结构与性质的叙述中正确的是( )
| A、CS2、H2O、C2H2都是直线形分子 |
| B、CH4、CCl4、SiH4都是含有极性键的非极性分子 |
| C、CH2=CH2和CH≡CH分子中含有的π键个数相等 |
| D、非极性键只存在于双原子的单质分子(如Cl2)中 |
考点:判断简单分子或离子的构型,极性分子和非极性分子
专题:化学键与晶体结构
分析:A、根据中心原子的杂化类型判断分子的空间构型;
B、不同非金属元素原子间易形成极性键,分子结构对称、正负电荷中心重叠的分子为非极性分子;
C、双键中含有1个π键,三键中含有2个π键;
D、同种非金属元素原子间易形成非极性键.
B、不同非金属元素原子间易形成极性键,分子结构对称、正负电荷中心重叠的分子为非极性分子;
C、双键中含有1个π键,三键中含有2个π键;
D、同种非金属元素原子间易形成非极性键.
解答:
解:A、CS2和C2H2的中心原子都只含有2个价层电子对,属于sp杂化,没有孤电子对,分子构型为直线形,H2O中O原子的价层电子对数=2+
(6-2×1)=4,属于sp3杂化,而且含有2 个孤电子对,分子的空间构型为V形,故A错误;
B、不同非金属元素原子间易形成极性键,分子结构对称、正负电荷中心重叠的分子为非极性分子,CH4、CCl4、SiH4都是含有极性键,CH4、CCl4、SiH4分子构型均为正四面体形,分子结构对称、正负电荷中心重叠属于非极性分子,故B正确;
C、双键中含有1个π键,三键中含有2个π键,则CH2=CH2中含有1个π键,CH≡CH分子中含有2个π键,二者的π键个数不相等,故C错误;
D、同种非金属元素原子间易形成非极性键,化合物中也可能存在非极性键,如CH2=CH2中C与C之间为非极性键,故D错误.
故选B.
| 1 |
| 2 |
B、不同非金属元素原子间易形成极性键,分子结构对称、正负电荷中心重叠的分子为非极性分子,CH4、CCl4、SiH4都是含有极性键,CH4、CCl4、SiH4分子构型均为正四面体形,分子结构对称、正负电荷中心重叠属于非极性分子,故B正确;
C、双键中含有1个π键,三键中含有2个π键,则CH2=CH2中含有1个π键,CH≡CH分子中含有2个π键,二者的π键个数不相等,故C错误;
D、同种非金属元素原子间易形成非极性键,化合物中也可能存在非极性键,如CH2=CH2中C与C之间为非极性键,故D错误.
故选B.
点评:本题考查了分子空间构型的判断、分子极性的判断、极性键和非极性键等,题目难度不大,侧重于基础知识的考查,注意把握价层电子对互斥理论的应用.

练习册系列答案
相关题目
四种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1:2,X2+和Z-离子的电子数之差为8.下列说法不正确的是( )
| A、与W相邻的同主族元素可制成重要的半导体材料 |
| B、元素原子半径从大到小的顺序是X、Y、Z |
| C、W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是H2YO4 |
| D、X的单质在W的最高价氧化物中的燃烧反应属于置换反应 |
已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:则下列说法或表达正确的是( )
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| A、CO2+H2O+2NaClO═Na2CO3+2HClO |
| B、2HCN+Na2CO3═CO2+2NaCN+H2O |
| C、常温下电离常数比较:Ka (H2CO3)>Ka(CH3COOH)>Ka(C6H5OH) |
| D、结合质子能力由强到弱的顺序为:CO2-3>HCO-3>CH3COO- |
下列离子方程式正确的是( )
A、用铜作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| B、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+═H2SiO3↓ | ||||
| C、H2O2溶液中加入稀硫酸和KI溶液:H2O2+2H++2I-═I2+2H2O | ||||
| D、Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
下列实验操作中存在有不合理操作的是( )
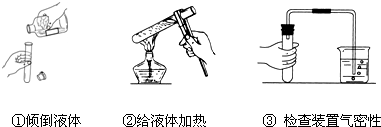

| A、①② | B、①③ | C、①②③ | D、②③ |
关于Na2CO3和NaHCO3的说法中正确的是( )
| A、为了将Na2CO3固体中的NaHCO3固体除去可以采用加热的方法 |
| B、Na2CO3溶液可以与Ca(OH)2溶液反应,而NaHCO3溶液不可以 |
| C、Na2CO3和NaHCO3都能与CaCl2溶液反应 |
| D、质量相同的Na2CO3 和NaHCO3与足量盐酸反应时所产生的CO2质量也相同 |
下列醇中能由醛还原制得的是( )
| A、CH3CH2CH2OH |
| B、(CH3)2CHCH(CH3)OH |
| C、(CH3)3COH |
| D、(CH3)2CHOH |
下列各组离子在溶液中能大量共存的是( )
A、Ba2+、Cl-、S
| ||
| B、K+、OH-、NO3-、Na+ | ||
| C、Ca2+、CO32-、Cl-、K+ | ||
| D、Ag+、NO3-、Cl-、K+ |
下列反应的离子方程式书写正确的是( )
| A、NaHCO3的水解:HCO3-+H2O?H3O++CO32- | ||||
| B、硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+=2Fe3++2H2O | ||||
| C、硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | ||||
D、除去KNO3溶液中的Fe3+:Fe3++3H2O
|