题目内容
3.用一种试剂除去下列各物质中的杂质(括号内为杂质),请写出相应的离子方程式.(1)Cu(Fe):离子方程式为Fe+2H+=Fe2++H2↑.
(2)CO2(HCl):离子方程式为H++HCO3-=H2O+CO2↑.
(3)MgO(Al2O3):离子方程式为Al2O3+2OH-═2AlO2-+H2O.
(4)O2(CO2):离子方程式CO2+2OH-═CO32-+H2O
(5)NaHCO3 (Na2CO3):离子方程式CO2+CO32-+H2O=2HCO3-.
分析 (1)Fe与盐酸反应,而Cu不能;
(2)HCl与饱和碳酸氢钠反应生成二氧化碳;
(3)氧化铝与NaOH反应,而MgO不能;
(4)二氧化碳与NaOH反应,而氧气不能;
(5)碳酸钠与二氧化碳、水反应生成碳酸氢钠.
解答 解:(1)Fe与盐酸反应,而Cu不能,离子反应为Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(2)HCl与饱和碳酸氢钠反应生成二氧化碳,离子反应为H++HCO3-=H2O+CO2↑,故答案为:H++HCO3-=H2O+CO2↑;
(3)氧化铝与NaOH反应,而MgO不能,离子反应为Al2O3+2OH-═2AlO2-+H2O,故答案为:Al2O3+2OH-═2AlO2-+H2O;
(4)二氧化碳与NaOH反应,而氧气不能,离子反应为CO2+2OH-═CO32-+H2O,故答案为:CO2+2OH-═CO32-+H2O;
(5)碳酸钠与二氧化碳、水反应生成碳酸氢钠,离子反应为CO2+CO32-+H2O=2HCO3-,故答案为:CO2+CO32-+H2O=2HCO3-.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力及混合物分离提纯考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
8.将一定量的CO2溶于100mL的0.4mol•L-1 KOH溶液.CO2被完全吸收,得到K2CO3和KHCO3的混合溶液.向所得溶液中逐滴加入0.2mol•L-1盐酸,至逸出的CO2与原先吸收的CO2质量相等.此时消耗的盐酸的体积为( )
| A. | 100 mL | B. | 200 mL | C. | 300 mL | D. | 400 mL |
15.下列说法正确的是( )
| A. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| B. | 石油裂解、煤的气化、海水制镁等过程中都包含化学变化 | |
| C. | 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源 | |
| D. | 通过化学变化可以实现235U与238U的相互转化 |
13.用纯碱固体配制一定物质的量浓度的该溶液时,不需要使用的玻璃仪器是( )
| A. | 玻璃棒 | B. | 胶头滴管 | C. | 容量瓶 | D. | 圆底烧瓶 |
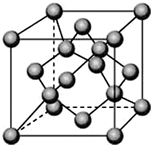 已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他3种元素既不在同一周期又不在同一主族.B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D原子的L层电子数与最外层电子数之比为4:1,其d轨道中有一对成对电子.请回答:
已知A、B、C、D都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他3种元素既不在同一周期又不在同一主族.B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D原子的L层电子数与最外层电子数之比为4:1,其d轨道中有一对成对电子.请回答: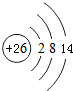 ,它的+3价离子的电子排布式为1s22s22p63s2sp5.
,它的+3价离子的电子排布式为1s22s22p63s2sp5. 实验室里要配制465mL 0.2mol/L的硫酸钠溶液.
实验室里要配制465mL 0.2mol/L的硫酸钠溶液.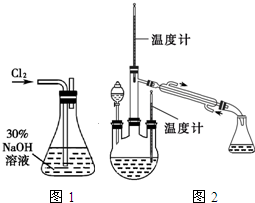 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).