题目内容
在体积为1L的密闭容器中发生反应2SO2(g)+O2(g)?2SO3(g).达到平衡后,若采用下列措施一段时间后,能增大逆反应速率的是( )
| A、体积不变,通入NO |
| B、增大容器容积 |
| C、体积不变,通入大量O2 |
| D、降低体系温度 |
考点:化学反应速率的影响因素
专题:
分析:增大反应的化学反应速率,可通过增大浓度、升高温度、使用催化剂等措施,对于气体参加的反应,还可以增大压强,据此分析.
解答:
解:A、通入NO能够与氧气反应,降低了反应物浓度,正逆反应速率都减小,故A错误;
B、增大容器体积,减小了反应物和生成物浓度,正逆反应速率都减小,故B错误;
C、容器体积不变,充入氧气,增大了反应物浓度,正逆反应速率都增大,故C正确;
D、降温,正逆反应速率都减小,故D错误;
故选C.
B、增大容器体积,减小了反应物和生成物浓度,正逆反应速率都减小,故B错误;
C、容器体积不变,充入氧气,增大了反应物浓度,正逆反应速率都增大,故C正确;
D、降温,正逆反应速率都减小,故D错误;
故选C.
点评:本题考查影响化学反应速率的因素,题目难度不大,注意影响反应速率的因素.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
下列有关实验现象的描述中,不正确的是( )
| A、灼烧Na与NaCl时,火焰颜色均显黄色 |
| B、钠在空气中燃烧后得到白色固体 |
| C、钠投入硫酸铜溶液中,会产生蓝色沉淀 |
| D、饱和碳酸钠溶液中滴加酚酞试液,溶液变红色 |
下列关于氯水的叙述中,正确的是( )
| A、新制氯水中只含Cl2和H2O分子 |
| B、光照氯水,有气体逸出,该气体为Cl2 |
| C、新制氯水可使蓝色石蕊试纸先变红后褪色 |
| D、氯水密封放置数天后pH将变大 |
反应3A+B=2C+D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L?s);②v(B)=0.06mol/(L?s);③v(C)=0.05mol/(L?s);④v(D)=0.045mol/(L?s).则反应进行由快到慢的顺序为( )
①v(A)=0.15mol/(L?s);②v(B)=0.06mol/(L?s);③v(C)=0.05mol/(L?s);④v(D)=0.045mol/(L?s).则反应进行由快到慢的顺序为( )
| A、④>③>①>② |
| B、②>④>③>① |
| C、②>①>④>③ |
| D、④>③>②>① |
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两上实验:N2O4?2NO2 △H>0,在以上两情况下,甲和乙容器的体积大小的比较,正确的是( )
(a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码.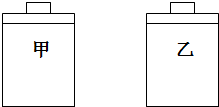
(a)将两容器置于沸水中加热
(b)在活塞上都加2kg的砝码.

| A、(a)甲>乙,(b)甲>乙 |
| B、(a)甲>乙,(b)甲=乙 |
| C、(a)甲<乙,(b)甲>乙 |
| D、(a)甲>乙,(b)甲<乙 |
分析如图所示的四个装置,其中结论正确的是( )
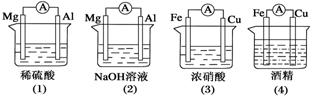

| A、(1)(2)中Mg作负极 |
| B、(3)中Fe作负极,电极反应为Fe-2e-═Fe2+ |
| C、(2)中Mg作正极,电极反应为6H2O+6e-═6OH-+3H2↑ |
| D、(4)中Fe作负极,电极反应为Fe-2e-═Fe2+ |
下列关于反应热的说法正确的是( )
| A、当△H为负值时,表示该反应为吸热反应 |
| B、燃烧不一定是放热反应 |
| C、反应热的大小与反应物所具有的能量和生成物具有的能量无关 |
| D、反应热的大小只与反应体系的始态和终态有关 |
以下是几种常用基本物理量的名称与符号的对应关系,其中不正确的是( )
| A、物质的量--mol |
| B、质量--m |
| C、时间--t |
| D、电流--I |