题目内容
 常见元素及其化合物在生活生产中有着广泛的应用.
常见元素及其化合物在生活生产中有着广泛的应用.(1)电解饱和食盐水可以制得重要的化工原料,其化学方程式为
(2)铁红与铝粉发生铝热反应可用于焊接钢轨,其化学方程式为
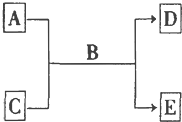
(3)几种常见的单质或化合物反应关系如图:
B为自然界中分布最广泛的液体,A常温下为黄绿色气体,C为非金属氧化物,A、C均能使品红溶液褪色,相对分子质量E>D,则:A、C转化为D、E反应的化学方程式为
考点:无机物的推断
专题:推断题
分析:(1)电解饱和食盐水生成氯气、氢气与氢氧化钠;制取漂白液利用氯气与碱反应得到氯化钠、次氯酸与水;
(2)铁红为氧化铁,与铝粉发生铝热反应所生产Fe与氧化铝;铁红与KNO3、KOH混合加热共融,可制得高铁酸钾(K2FeO4),同时有KNO2生成,根据元素守恒可知有水生成,配平书写方程式;K2FeO4具有强氧化性,可杀菌消毒;还原产物可吸附水中杂质;
(3)B为自然界中分布最广泛的液体,应为H2O,A常温下为黄绿色气体,C为非金属氧化物,A、C均能使品红溶液褪色,则A为Cl2,C为SO2,反应得到HCl与H2SO4,相对分子质量E>D,则D为HCl、E为H2SO4,Cu与浓硫酸反应得到硫酸铜、二氧化硫与水.
(2)铁红为氧化铁,与铝粉发生铝热反应所生产Fe与氧化铝;铁红与KNO3、KOH混合加热共融,可制得高铁酸钾(K2FeO4),同时有KNO2生成,根据元素守恒可知有水生成,配平书写方程式;K2FeO4具有强氧化性,可杀菌消毒;还原产物可吸附水中杂质;
(3)B为自然界中分布最广泛的液体,应为H2O,A常温下为黄绿色气体,C为非金属氧化物,A、C均能使品红溶液褪色,则A为Cl2,C为SO2,反应得到HCl与H2SO4,相对分子质量E>D,则D为HCl、E为H2SO4,Cu与浓硫酸反应得到硫酸铜、二氧化硫与水.
解答:
解:(1)电解饱和食盐水生成氯气、氢气与氢氧化钠,反应方程式为:2NaCl+2H2O
Cl2↑+H2↑+2NaOH,制取漂白液利用氯气与碱反应得到氯化钠、次氯酸与水,离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:2NaCl+2H2O
Cl2↑+H2↑+2NaOH;Cl2+2OH-=Cl-+ClO-+H2O;
(2)铁红为氧化铁,与铝粉发生铝热反应所生产Fe与氧化铝,反应方程式为:2Al+Fe2O3
Al2O3+2Fe;氧化铁与KNO3、KOH混合加热共融,可制得高铁酸钾(K2FeO4),同时有KNO2生成,根据元素守恒可知有水生成,反应方程式为:Fe2O3+3KNO3+4KOH
2K2FeO4+3KNO2+2H2O;K2FeO4具有强氧化性,可杀菌消毒;还原产物可吸附水中杂质,
故答案为:2Al+Fe2O3
Al2O3+2Fe;Fe2O3+3KNO3+4KOH
2K2FeO4+3KNO2+2H2O;K2FeO4具有强氧化性,可杀菌消毒;还原产物可吸附水中杂质;
(3)B为自然界中分布最广泛的液体,应为H2O,A常温下为黄绿色气体,C为非金属氧化物,A、C均能使品红溶液褪色,则A为Cl2,C为SO2,反应得到HCl与H2SO4,反应方程式为:Cl2+SO2+2H2O=2HCl+H2SO4,相对分子质量E>D,则D为HCl、E为H2SO4,浓硫酸溶液与Cu反应到硫酸铜、二氧化硫与水,反应化学方程式为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
故答案为:Cl2+SO2+2H2O=2HCl+H2SO4;Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O.
| ||
故答案为:2NaCl+2H2O
| ||
(2)铁红为氧化铁,与铝粉发生铝热反应所生产Fe与氧化铝,反应方程式为:2Al+Fe2O3
| ||
| ||
故答案为:2Al+Fe2O3
| ||
| ||
(3)B为自然界中分布最广泛的液体,应为H2O,A常温下为黄绿色气体,C为非金属氧化物,A、C均能使品红溶液褪色,则A为Cl2,C为SO2,反应得到HCl与H2SO4,反应方程式为:Cl2+SO2+2H2O=2HCl+H2SO4,相对分子质量E>D,则D为HCl、E为H2SO4,浓硫酸溶液与Cu反应到硫酸铜、二氧化硫与水,反应化学方程式为:Cu+2H2SO4(浓)
| ||
故答案为:Cl2+SO2+2H2O=2HCl+H2SO4;Cu+2H2SO4(浓)
| ||
点评:本题考查无机物推断,涉及Fe、Al、Cl、S元素单质化合物性质及氯碱工业等,学生学生熟练掌握元素化合物性质,难度不大,注意对基础知识的掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 下列选项中,符合如图所示关系的是( )
下列选项中,符合如图所示关系的是( )| A、一定状况下,气体摩尔体积(Y)与该气体的物质的量(X)的关系 |
| B、Fe在Cl2中燃烧,生成FeCl3的物质的量(Y)与消耗Cl2物质的量(X)的关系 |
| C、燃烧一定质量C2H4与C3H6的混合气体,消耗O2的物质的量(Y)与C3H6的质量分数(X)的关系 |
| D、H2SO4溶液的物质的量浓度(Y)与其质量分数(X)的关系 |

 某课外兴趣小组用如图装置进行实验,试回答:
某课外兴趣小组用如图装置进行实验,试回答: )发生酯化反应的产物.
)发生酯化反应的产物.