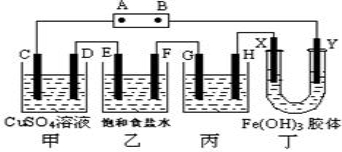
题目内容
下列离子反应方程式正确的是
A.氯气溶于水:Cl2+H2O═2H++ Cl﹣+ClO-
B.Fe2+与NO3-在酸性溶液中的反应: Fe2++NO3-+4H+=Fe3++NO↑+2H2O
C.稀硫酸和Ba(OH)2溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.浓 硝酸中加入铜片: Cu+4H++2NO3-═Cu2++2NO2↑+2H2O
硝酸中加入铜片: Cu+4H++2NO3-═Cu2++2NO2↑+2H2O
练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
已知A(g)+B(g) 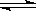 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005 mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.76 mol/L
B.830℃达平衡时,A的转化率为80%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g) 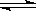 A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4


 D.无法判断
D.无法判断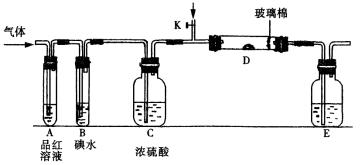



 Cl2↑+ H2↑+ 2OH-
Cl2↑+ H2↑+ 2OH-