题目内容
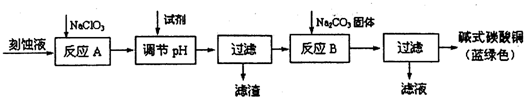
铝土矿的主要成分是Al2O3和杂质SiO2、Fe2O3等.从铝土矿中提炼Al2O3的流程如下:
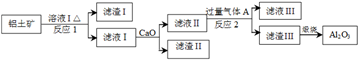
滤液III主要溶质能用于泡沫灭火器,回答下列问题:
(1)电解制铝的阴极材料是(钢板、石墨) ,阳极电极反应式 .
(2)溶液I溶质的化学式是 ,溶液I如用盐酸,缺点1是(离子方程式表示) ,
缺点2是 .
(3)滤液III主要溶质的俗名是 .
(4)上述滤渣I~III中,有一种的主要成分与水泥的主要成分之一相同,该物质是 ,为了反应快速、完全,过滤之前还应有的操作是 .

滤液III主要溶质能用于泡沫灭火器,回答下列问题:
(1)电解制铝的阴极材料是(钢板、石墨)
(2)溶液I溶质的化学式是
缺点2是
(3)滤液III主要溶质的俗名是
(4)上述滤渣I~III中,有一种的主要成分与水泥的主要成分之一相同,该物质是
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:铝土矿的主要成分Al2O3和杂质SiO2、Fe2O3等,由流程可知,滤液Ⅱ通入过量气体A得到滤液Ⅲ与滤渣Ⅲ,滤渣Ⅲ煅烧得到氧化铝,滤液Ⅲ主要溶质能用于泡沫灭火器,故滤渣Ⅲ为Al(OH)3,气体A应该为CO2,滤液Ⅲ主要溶质为NaHCO3,滤液Ⅰ与CaO处理后得到偏铝酸盐,由于氢氧化钙的溶解性较小,不适合将铝离子转化为偏铝酸根,故滤液Ⅱ中Al元素以偏铝酸根形式存在,则溶液Ⅰ为强碱,应是NaOH,故滤渣Ⅰ为Fe2O3,滤液Ⅰ中含有硅酸钠、偏铝酸钠及过量的NaOH,经CaO处理后得到滤渣Ⅱ为CaSiO3.
(1)电解熔融氧化铝制备铝,氧离子在阳极失去电子生成氧气,阳极材料易与氧气反应,容易损耗,而阴极不反应,考虑经济效益,阴极为钢板、阳极为石墨;
(2)溶液I如用盐酸,盐酸可以与氧化铁反应生成氯化铁,且盐酸易挥发,且用CaO处理滤液Ⅰ时,Al元素会部分转化为沉淀,Al元素利用率降低;
(3)滤液Ⅲ主要溶质为NaHCO3;
(4)水泥的主要成分为硅酸盐;为了反应快速、完全,过滤之前通常进行搅拌.
(1)电解熔融氧化铝制备铝,氧离子在阳极失去电子生成氧气,阳极材料易与氧气反应,容易损耗,而阴极不反应,考虑经济效益,阴极为钢板、阳极为石墨;
(2)溶液I如用盐酸,盐酸可以与氧化铁反应生成氯化铁,且盐酸易挥发,且用CaO处理滤液Ⅰ时,Al元素会部分转化为沉淀,Al元素利用率降低;
(3)滤液Ⅲ主要溶质为NaHCO3;
(4)水泥的主要成分为硅酸盐;为了反应快速、完全,过滤之前通常进行搅拌.
解答:
解:铝土矿的主要成分Al2O3和杂质SiO2、Fe2O3等,由流程可知,滤液Ⅱ通入过量气体A得到滤液Ⅲ与滤渣Ⅲ,滤渣Ⅲ煅烧得到氧化铝,滤液Ⅲ主要溶质能用于泡沫灭火器,故滤渣Ⅲ为Al(OH)3,气体A应该为CO2,滤液Ⅲ主要溶质为NaHCO3,滤液Ⅰ与CaO处理后得到偏铝酸盐,由于氢氧化钙的溶解性较小,不适合将铝离子转化为偏铝酸根,故滤液Ⅱ中Al元素以偏铝酸根形式存在,则溶液Ⅰ为强碱,应是NaOH,故滤渣Ⅰ为Fe2O3,滤液Ⅰ中含有硅酸钠、偏铝酸钠及过量的NaOH,经CaO处理后得到滤渣Ⅱ为CaSiO3.
(1)电解熔融氧化铝制备铝,氧离子在阳极失去电子生成氧气,阳极电极反应式为:2O2--4e-=O2↑,阳极材料易与氧气反应,容易损耗,而阴极不反应,考虑经济效益,阴极为钢板、阳极为石墨,
故答案为:钢板;2O2--4e-=O2↑;
(2)有上述分析可知,溶液I溶质的化学式是NaOH;溶液I如用盐酸,盐酸可以与氧化铁反应生成氯化铁,反应;反应离子方程式为:Fe2O3+6H+=2Fe3++3H2O,且盐酸易挥发,污染空气,浪费原料,且用CaO处理滤液Ⅰ时,Al元素会部分转化为沉淀,Al元素利用率降低,
故答案为:NaOH;Fe2O3+6H+=2Fe3++3H2O;盐酸易挥发,污染空气,浪费原料;
(3)滤液Ⅲ主要溶质为NaHCO3,俗称小苏打,故答案为:小苏打;
(4)水泥的主要成分为硅酸盐,故滤渣I~III中CaSiO3与水泥的主要成分之一相同,为了反应快速、完全,过滤之前还应有的操作是搅拌,
故答案为:CaSiO3;搅拌.
(1)电解熔融氧化铝制备铝,氧离子在阳极失去电子生成氧气,阳极电极反应式为:2O2--4e-=O2↑,阳极材料易与氧气反应,容易损耗,而阴极不反应,考虑经济效益,阴极为钢板、阳极为石墨,
故答案为:钢板;2O2--4e-=O2↑;
(2)有上述分析可知,溶液I溶质的化学式是NaOH;溶液I如用盐酸,盐酸可以与氧化铁反应生成氯化铁,反应;反应离子方程式为:Fe2O3+6H+=2Fe3++3H2O,且盐酸易挥发,污染空气,浪费原料,且用CaO处理滤液Ⅰ时,Al元素会部分转化为沉淀,Al元素利用率降低,
故答案为:NaOH;Fe2O3+6H+=2Fe3++3H2O;盐酸易挥发,污染空气,浪费原料;
(3)滤液Ⅲ主要溶质为NaHCO3,俗称小苏打,故答案为:小苏打;
(4)水泥的主要成分为硅酸盐,故滤渣I~III中CaSiO3与水泥的主要成分之一相同,为了反应快速、完全,过滤之前还应有的操作是搅拌,
故答案为:CaSiO3;搅拌.
点评:本题考查物质分离和提纯,侧重考查铝及其化合物的性质,正确理解流程图中各个步骤反应原理及基本操作是解本题关键,同时考查学生分析问题、基本操作及灵活运用知识解答问题能力,综合性较强,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关物质的量的说法中,正确的是( )
| A、Mg的摩尔质量为24g |
| B、物质的量的单位是摩尔 |
| C、1 mol O2在任何条件下的体积都为22.4L |
| D、将1 mol NaCl晶体加入到1L水中,得到NaCl溶液的浓度就是1 mol?L-1 |
一定量某营养液中溶质的配方分别如下:对于两种营养液的成分,下列说法中正确的是( )
配方一:0.3mol KCl,0.2mol K2SO4,0.1molZnSO4
配方二:0.1mol KCl,0.3mol K2SO4,0.1molZnCl2.
配方一:0.3mol KCl,0.2mol K2SO4,0.1molZnSO4
配方二:0.1mol KCl,0.3mol K2SO4,0.1molZnCl2.
| A、只有n(K+)相同 |
| B、只有n(Cl-)相同 |
| C、各离子的物质的量完全不同 |
| D、完全相同 |