题目内容
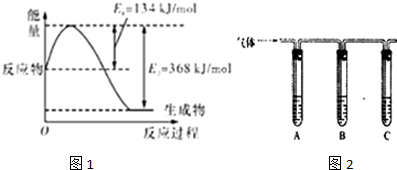
(1)随着大气污染的日趋严重,“节能减排”,减少全球温室气体排放,研究NOx、SO2、CO等大气污染气体的处理具体有重要意义.如图1是在101kPa,298K条件下1mol NO2和1mol CO反应生成1mol CO2和1mol NO过程中的能量变化示意图.已知:
①N2(g)+O2(g)═2NO(g)△H=+179.5kJ/mol
②2NO(g)+O 22(g)═2NO2(g)△═-112.3kJ/mol
请写出NO与CO反应生成无污染气体的热化学方程式: .
(2)某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O.某学习小组拟探究该消毒液的变质情况.
Ⅰ.取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过下列如2装置检验气体的成分可以判断消毒液是否变质.
学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙: .[来源:学科王
为了验证可能为甲,请完成下列实验方案.限选 试剂:
①98%的浓硫酸 ②1%的品红溶液 ③1.0mol/L的KI-淀粉溶液 ④1.0mol/L的NaOH溶液 ⑤澄清石灰水 ⑥饱和NaCl溶液
Ⅱ.用滴定法测定消毒液中NaClO的浓度(滴定过程涉及的反应有:
NaClO+Na2SO3=NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O).
实验步骤如下:
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol/L Na2SO3溶液V1 mL;
②在使用滴定管之前首先进行的操作是 ;将b mol/L的酸性KMnO4溶液装入 滴定管(填“酸式”或“碱式”)中;滴定,KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且保持半分钟内红色不褪时,停止滴定,记录数据.
③重复滴定操作2次,平均消耗酸性KMnO4溶液 V2 mL.则消毒液中NaClO的浓度为 mol/L(用含a、b、V1、V2的代数式表示).

①N2(g)+O2(g)═2NO(g)△H=+179.5kJ/mol
②2NO(g)+O 22(g)═2NO2(g)△═-112.3kJ/mol
请写出NO与CO反应生成无污染气体的热化学方程式:
(2)某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O.某学习小组拟探究该消毒液的变质情况.
Ⅰ.取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过下列如2装置检验气体的成分可以判断消毒液是否变质.
学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙:
为了验证可能为甲,请完成下列实验方案.限选 试剂:
①98%的浓硫酸 ②1%的品红溶液 ③1.0mol/L的KI-淀粉溶液 ④1.0mol/L的NaOH溶液 ⑤澄清石灰水 ⑥饱和NaCl溶液
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量 试管B中加1%品红溶液; 试管C中加 | 若 |
NaClO+Na2SO3=NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O).
实验步骤如下:
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol/L Na2SO3溶液V1 mL;
②在使用滴定管之前首先进行的操作是
③重复滴定操作2次,平均消耗酸性KMnO4溶液 V2 mL.则消毒液中NaClO的浓度为
考点:常见的生活环境的污染及治理,热化学方程式,中和滴定
专题:
分析:(1)依据图象写出热化学方程式,结合题干热化学方程式和盖斯定律计算得到所需让化学方程式;
(2)Ⅰ、由甲:部分变质;乙:未变质,猜测丙中可能全部变质;
若验证部分变质,则检验氯气、碳酸钠均存在即可,以此选择试剂,结合发生的化学反应分析现象;
Ⅱ、②滴定管使用之前需要查漏,酸性KMnO4溶液具有氧化性,能氧化橡胶管;
③由NaClO+Na2SO3=NaCl+Na2SO4、2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O可知,以此计算.
(2)Ⅰ、由甲:部分变质;乙:未变质,猜测丙中可能全部变质;
若验证部分变质,则检验氯气、碳酸钠均存在即可,以此选择试剂,结合发生的化学反应分析现象;
Ⅱ、②滴定管使用之前需要查漏,酸性KMnO4溶液具有氧化性,能氧化橡胶管;
③由NaClO+Na2SO3=NaCl+Na2SO4、2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O可知,以此计算.
解答:
解:(1)①N2(g)+O2(g)=2NO(g)△H=+179.5kJ/mol
②2NO(g)+O2(g)=2NO2(g)△H=-112.3kJ/mol
依据图象书写得到热化学方程式③NO2(g)+CO(g)=CO2(g)+NO(g)△H=(134-368)KJ/mol=-234KJ/mol;
由盖斯定律②+③-①得到反应的热化学方程式:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-759.8KJ/mol,
故答案为:2NO(g)+2CO(g)?N2(g)+2CO2(g)的△H=-759.8KJ/mol;
(2)Ⅰ、由甲:部分变质;乙:未变质,猜测丙中可能全部变质,即丙为全部变质;
若验证部分变质,则检验氯气、碳酸钠均存在即可,检验氯气,选择③1.0mol?L-1 的KI-淀粉溶液,生成碘单质溶液变蓝,证明存在氯气,
检验碳酸钠,选择⑤澄清石灰水,生成的二氧化碳使石灰水变浑浊,所以A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,说明甲正确,
故答案为:全部变质;
;
Ⅱ、②滴定管使用之前需要检查是否漏液,酸性KMnO4溶液具有氧化性,能氧化橡胶管,则应选用酸式滴定管,故答案为:检查滴定管是否漏液(或检漏);酸式;
③由NaClO+Na2SO3=NaCl+Na2SO4、2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O可知,
2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O
2 5
bv2×0.001
设消毒液中NaClO的浓度为x,则
5NaClO~2KMnO4
5 2
0.025x 0.001av1-
解得x=
mol/L,
故答案为:
mol/L.
②2NO(g)+O2(g)=2NO2(g)△H=-112.3kJ/mol
依据图象书写得到热化学方程式③NO2(g)+CO(g)=CO2(g)+NO(g)△H=(134-368)KJ/mol=-234KJ/mol;
由盖斯定律②+③-①得到反应的热化学方程式:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-759.8KJ/mol,
故答案为:2NO(g)+2CO(g)?N2(g)+2CO2(g)的△H=-759.8KJ/mol;
(2)Ⅰ、由甲:部分变质;乙:未变质,猜测丙中可能全部变质,即丙为全部变质;
若验证部分变质,则检验氯气、碳酸钠均存在即可,检验氯气,选择③1.0mol?L-1 的KI-淀粉溶液,生成碘单质溶液变蓝,证明存在氯气,
检验碳酸钠,选择⑤澄清石灰水,生成的二氧化碳使石灰水变浑浊,所以A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,说明甲正确,
故答案为:全部变质;
| ③; ⑤ | A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊 |
Ⅱ、②滴定管使用之前需要检查是否漏液,酸性KMnO4溶液具有氧化性,能氧化橡胶管,则应选用酸式滴定管,故答案为:检查滴定管是否漏液(或检漏);酸式;
③由NaClO+Na2SO3=NaCl+Na2SO4、2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O可知,
2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O
2 5
| 2bv2×0.001 |
| 5 |
设消毒液中NaClO的浓度为x,则
5NaClO~2KMnO4
5 2
0.025x 0.001av1-
| 2bv2×0.001 |
| 5 |
aV1-
| ||
| 25 |
故答案为:
aV1-
| ||
| 25 |
点评:本题考查了热化学方程式和盖斯定律计算应用及以消毒液考查物质的成分及含量的探究,明确物质的性质及发生的化学反应为解答的关键,注意计算中量的关系为解答的易错点,验证甲为解答的难点,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、氯乙烷与浓硫酸混和加热到170℃可发生消去反应生成乙烯 |
| B、苯与浓硝酸、浓硫酸的混和物加热到100~110℃时,因浓硝酸挥发和分解而得不到硝化产物 |
| C、将苯酚、40%的甲醛溶液和少量浓盐酸混和,水浴加热数分钟即可生成酚醛树脂 |
| D、酯化反应通常需要在浓硫酸存在下进行,浓硫酸此时既是催化剂又是吸水剂 |
下列反应中,水既不作氧化剂又不作还原剂的氧化还原反应是( )
| A、钠与水反应 |
| B、氧化钠与水反应 |
| C、过氧化钠与水反应 |
| D、二氧化硫与水反应 |
下列各组物质中,属于同分异构体的是( )
| A、O2和O3 |
| B、CH2=CHCH2CH3和CH3CH=CHCH3 |
| C、CH3CH2CH3和CH3(CH2)2CH3 |
| D、乙醇和乙醚 |
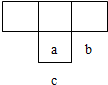 短周期元素a、b、c在周期表中位置如图所示,已知三者原子序数之和为27,则a、b、C三种元素的名称是( )
短周期元素a、b、c在周期表中位置如图所示,已知三者原子序数之和为27,则a、b、C三种元素的名称是( )| A、碳、氮、硅 |
| B、氮、氧、磷 |
| C、硼、碳、铝 |
| D、氧、氟、硫 |
下列说法不正确的是( )
| A、《京都议定书》针对六种温室气体进行削减,包括二氧化碳(CO2)、甲烷(CH4)、氧化亚氮(N2O)、氢氟碳化物(HFCs)、全氟碳化物(PFCs)及六氟化硫(SF6).科学研究发现,同条件下等体积的甲烷产生的温室效应远远强于二氧化碳的.那么等质量的二氧化碳产生温室效应比甲烷的强 |
| B、合成高学科王效、稳定、廉价的太阳能光电转化材料,是开发利用太阳能的关键 |
| C、稀土元素都是长周期元素,稀土资源是国家战略性资源 |
| D、环境问题的最终解决要依靠科技进步,通常利用沉淀反应除去污水中的重金属离子 |
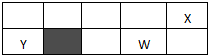 已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( )
已知:X、Y、Z、W为短周期元素,原子半径X:99pm Y:154pm Z:125pm W:117pm,X、Y、W位置如图所示(副族省略),X、Y、Z的最高价氧化物对应的水化物相互能反应,下列说法正确的是( )| A、元素Z处于周期表的阴影位置 |
| B、X与W形成的化合物熔点很高,为离子化合物 |
| C、X、W的最高价氧化物对应水化物的酸性:X>W |
| D、Y、W的最高价氧化物的晶体类型相同 |
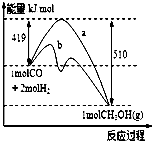 工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g)
工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g)