题目内容
4.水杨酸是合成阿斯匹林的重要原料.水杨酸的学名邻羟基苯甲酸,结构简式为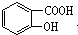 ,请回答下列问题:
,请回答下列问题:(1)请写出水杨酸中除苯环外具有的官能团羧基和酚羟基.
(2)请写出与水杨酸互为同分异构体,既属于酚类又属于醛类化合物的结构简式(写一种即可):
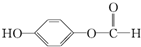 .
.(3)水杨酸的另一种同分异构体的结构简式为
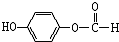 ,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)C;
,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)C;A.1mol B.2mol C.3mol D.4mol.
(4)已知有机物CH3COOH可以表示为:
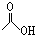 ,在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林可表示为:
,在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林可表示为: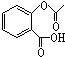 ,则阿斯匹林的分子式为C9H8O4.
,则阿斯匹林的分子式为C9H8O4.(5)阿斯匹林药片需要保存在干燥处,受潮的药片易变质不宜服用;检验受潮药片是否变质的试剂是(只选一种试剂即可)氯化铁溶液.
分析  含有羧基,具有酸性,可发生中和、酯化反应,含有羟基,可发生取代、氧化和显色反应,结合官能团的性质以及题目要求解答该题.
含有羧基,具有酸性,可发生中和、酯化反应,含有羟基,可发生取代、氧化和显色反应,结合官能团的性质以及题目要求解答该题.
解答 解:(1)水杨酸中含有官能团名称是羧基和酚羟基,故答案为:羧基和酚羟基;
(2)水杨酸 的同分异构体符合含酚羟基,且含有醛基的所有同分异构体可为
的同分异构体符合含酚羟基,且含有醛基的所有同分异构体可为 等,也可含有1个醛基、2个羟基,
等,也可含有1个醛基、2个羟基,
故答案为: 等;
等;
(3)能和氢氧化钠反应的有酚羟基和酯基水解生成的酚羟基和羧基,所以1mol该有机物 在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为3mol,故选C;
在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为3mol,故选C;
(4)有机物CH3COOH可以表示为: ,在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林可表示为:
,在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林可表示为: ,则阿斯匹林的分子式为C9H8O4,故答案为:C9H8O4;
,则阿斯匹林的分子式为C9H8O4,故答案为:C9H8O4;
(5)阿司匹林变质时发生水解反应生成酚羟基,所以可以用氯化铁溶液检验,故答案为:氯化铁溶液.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系是解本题关键,侧重考查羧酸和、酯、酚的性质,注意酯基水解生成的酚羟基也能和氢氧化钠反应,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列反应的离子方程式书写正确的是( )
| A. | 用小苏打治疗胃酸过多2H++CO32-═CO2↑+H2O | |
| B. | 用氢氧化钠溶液除去铝表面的氧化膜 Al2O3+2OH-═2AlO2-+H2O | |
| C. | 氯化亚铁溶液通入氯气 Fe2++Cl2═Fe3++2Cl- | |
| D. | 用食醋除去水瓶中的水垢 CO32-+2H+═H2O+CO2↑ |
15.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X单质的还原性大于Y的单质的还原性.下列说法正确的是( )
| A. | W与X形成的化合物中只含离子键 | |
| B. | W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 | |
| C. | X、Y、Z、W的原子半径依次减小 | |
| D. | 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
12.有机物X(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,该化合物具有如下性质:
(1)1molX与足量的金属钠反应产生1.5mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应根据上述信息
对X的结构判断正确的是( )
(1)1molX与足量的金属钠反应产生1.5mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应根据上述信息
对X的结构判断正确的是( )
| A. | X中可能有两个羧基和一个羟基 | |
| B. | X中可能有三个羟基和一个 一COOR官能团 | |
| C. | X中肯定有碳碳双键 | |
| D. | X中可能有三个羧基 |
9.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在0.1molNaHSO4晶体中阳离子与阴离子总数为0.3NA | |
| B. | 1.0L0.1mol•L-1NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023 | |
| C. | 7.8gNa2O2与足量CO2反应,转移的电子数为0.1NA | |
| D. | 向仅含0.2molFeI2的溶液中持续通入氯气,当有0.1molFe2+被氧化时,需通入标况下C121.12L |
16.已知室温下,某溶液中由水电离出的H+和OH-的物质的量浓度的乘积约为1×10-24,则在该溶液中,一定能大量存在的离子是( )
| A. | NH4+ | B. | NO3- | C. | AlO2- | D. | HCO3- |
13.Ⅰ:工业制硫酸时,利用接触氧化反应将SO 2转化为SO3是一个关键步骤.
(1)某温度下,2SO2(g)+O 2(g)?2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0mol O 2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)在硫酸工业生产过程中,有反应2SO2(g)+O2(g)?2SO3(g)(正反应为放热反应),根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件(以V2O5作催化剂)温度450℃;压强1×105Pa.
(4)能判断该反应达到平衡状态的依据是ACF.
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO 3的浓度不变 D.C(SO 2)=C(SO 3)
E.v 正(SO 2)=v 正(SO 3) F.v 正(SO 3)=2v 逆(O 2)
Ⅱ:研究化学反应原理对于生产生活是很有意义的.
(1)在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=2.2×10-8mol•L-1(Ksp[Cu(OH)2]=2.2×10-20).
(2)若在0.1mol•L-1硫酸铜溶液中通入H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是0.2mol•L-1.
(1)某温度下,2SO2(g)+O 2(g)?2SO3(g)△H=-197kJ/mol.开始时在10L的密闭容器中加入8.0mol SO2(g)和20.0mol O 2(g),当反应达到平衡时共放出394kJ的热量,该温度下的平衡常数K=0.56(保留两位有效数字),若升高温度时,K将减小(填“增大、减小或不变”).
(2)若体积不变的条件下,下列措施中有利于提高SO2的转化率条件是AC(填字母).
A.通入氧气 B.移出氧气 C.增大压强 D.减小压强 E.加入催化剂
(3)在硫酸工业生产过程中,有反应2SO2(g)+O2(g)?2SO3(g)(正反应为放热反应),根据下表提供的不同条件下SO2的转化率(%)的数据,试选择该反应的适宜条件(以V2O5作催化剂)温度450℃;压强1×105Pa.
| 1×105Pa | 5×105Pa | 10×105Pa | 50×105Pa | 100×105Pa | |
| 450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.容器的压强不变 B.混合气体的密度不变
C.混合气体中SO 3的浓度不变 D.C(SO 2)=C(SO 3)
E.v 正(SO 2)=v 正(SO 3) F.v 正(SO 3)=2v 逆(O 2)
Ⅱ:研究化学反应原理对于生产生活是很有意义的.
(1)在0.10mol•L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=2.2×10-8mol•L-1(Ksp[Cu(OH)2]=2.2×10-20).
(2)若在0.1mol•L-1硫酸铜溶液中通入H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是0.2mol•L-1.
14.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 25℃时,1L pH=ll的CH3COONa溶液中水电离出的OH-的数目为0.001NA | |
| B. | 28g乙烯和丙烯的混合气体含有的原子个数为3NA | |
| C. | 1 mol/L-l NaHCO3溶液中含有HCO3-数目小于NA | |
| D. | 6.8g液态KHSO4中含有0.1NA个阳离子 |
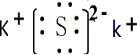 ,属于离子晶体.
,属于离子晶体.