题目内容
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )


| A、a和b不连接时,铁片上发生的反应为:Cu2++Fe═Cu+Fe2+ |
| B、a和b用导线连接时,Cu2+向铁电极移动 |
| C、a和b分别连接直流电源正、负极,铜片会溶解 |
| D、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
考点:原电池和电解池的工作原理
专题:
分析:A.铁较活泼,可置换出铜;
B.形成原电池反应时,阳离子向正极移动;
C.铜如为阳极,则被氧化;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+.
B.形成原电池反应时,阳离子向正极移动;
C.铜如为阳极,则被氧化;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+.
解答:
解:A.a和b不连接时,发生Fe+Cu2+=Cu+Fe2+置换反应,则铁片上会有金属铜析出,故A正确;
B.a和b用导线连接时,形成原电池反应,a为正极,阳离子向正极移动,即向铜移动,故B错误;
C.铜为阳极,被氧化而溶解,故C正确;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+,则铁片均溶解,溶液从蓝色逐渐变成浅绿色,故D正确;
故选B.
B.a和b用导线连接时,形成原电池反应,a为正极,阳离子向正极移动,即向铜移动,故B错误;
C.铜为阳极,被氧化而溶解,故C正确;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+,则铁片均溶解,溶液从蓝色逐渐变成浅绿色,故D正确;
故选B.
点评:本题考查原电池和电解池,为高频考点,明确原电池及电解池的中发生的电极反应、电极判断及发生的总反应即可解答,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
下列最简式中,没有相对分子质量也可以确定分子式的是( )
| A、CH3 |
| B、CH |
| C、CH2 |
| D、CH2O |
在反应 2H2S+SO2=3S↓+2H2O 中,还原剂与氧化剂的物质的量之比为( )
| A、1:2 | B、2:1 |
| C、1:1 | D、3:2 |
下列有关电化学的说法正确的是( )
| A、燃料电池是将燃料燃烧产生的热能直接转变为电能 |
| B、铅蓄电池在放电时,正极发生的反应是 Pb(s)+SO42-(aq)=PbSO4(s)+2e- |
| C、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 |
| D、钢铁电化学腐蚀的两种类型主要区别在于水膜的pH不同,引起的正极反应不同 |
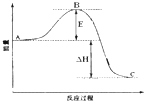 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.下列说法正确的是( )
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ?mol-1.下列说法正确的是( )| A、图中A、C分别表示反应物总能量和生成物总能量 | ||
| B、加入催化剂,图中E和△H都减小 | ||
| C、图中△H=-99kJ?mol-1 | ||
D、SO3(g)?
|
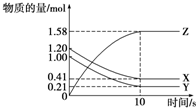 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )| A、反应开始到10 s,用Z表示的平均反应速率为0.158 mol?L-1?s-1 |
| B、反应开始到10 s,X的物质的量浓度减少了0.79 mol?L-1 |
| C、反应开始到10 s,Y的物质的量浓度减少了0.395 mol?L-1 |
| D、反应的化学方程式为X(g)+Y(g)?Z(g) |