题目内容
下列说法正确的是( )
| A、电解饱和食盐水时,阳极析出氢气 |
| B、在船身装上锌块利用的是牺牲阳极的阴极保护法 |
| C、钢铁发生吸氧腐蚀负极的电极反应式是2H2O+O2+4e-=4OH- |
| D、电解精炼铜时,杂质Fe、Zn、Ag等沉积在电解槽底部 |
考点:金属的电化学腐蚀与防护,电解原理
专题:电化学专题
分析:A、电解时阳极阴离子放电;
B、Zn、Fe形成原电池时Zn被腐蚀;
C、原电池中负极失电子;
D、电解池的阳极上活泼性强的金属先失电子.
B、Zn、Fe形成原电池时Zn被腐蚀;
C、原电池中负极失电子;
D、电解池的阳极上活泼性强的金属先失电子.
解答:
解:A、电解时阳极阴离子放电,则电解饱和食盐水时,氯离子阳极失电子生成氯气,故A错误;
B、Zn、Fe形成原电池时Zn被腐蚀,Fe被保护,此法为牺牲阳极的阴极保护法,故B正确;
C、原电池中负极失电子,则钢铁发生吸氧腐蚀负极的电极反应式是Fe-2e-=Fe2+,故C错误;
D、电解池的阳极上活泼性强的金属先失电子,Fe、Zn的活泼性比铜强,在阳极上失电子生成离子,活泼性比铜弱的金属Ag等沉积在电解槽底部,故D错误.
故选B.
B、Zn、Fe形成原电池时Zn被腐蚀,Fe被保护,此法为牺牲阳极的阴极保护法,故B正确;
C、原电池中负极失电子,则钢铁发生吸氧腐蚀负极的电极反应式是Fe-2e-=Fe2+,故C错误;
D、电解池的阳极上活泼性强的金属先失电子,Fe、Zn的活泼性比铜强,在阳极上失电子生成离子,活泼性比铜弱的金属Ag等沉积在电解槽底部,故D错误.
故选B.
点评:本题考查了电解原理的应用、金属的电化学防护、原电池原理等,侧重于考查基础知识的应用,属于基础性题目,难度不大,注意相关知识的积累.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
分子式为C4H8O2,且能发生水解反应的有机物有(不考虑立体异构)( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列有关化学用语或名称表达正确的是( )
A、Mg的原子结构示意图: |
B、乙炔的分子结构模型示意图: |
C、H2O2的电子式: |
D、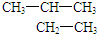 的名称:2-甲基丁烷 的名称:2-甲基丁烷 |
已知在3.2g某气体中所含分子数目为3.01×1022,由此可推知该气体的摩尔质量是( )
| A、64g |
| B、32g?mol-1 |
| C、32g |
| D、64 g?mol-1 |
 一定质量的Na.K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a.b所示,则下列说法中正确的是( )
一定质量的Na.K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a.b所示,则下列说法中正确的是( )| A、投入的Na.K物质的质量一定相等 |
| B、曲线a对应的反应使用了催化剂 |
| C、曲线a代表K的反应,曲线b代表Na |
| D、两反应中盐酸必须是足量的 |
下列关于主族元素性质的递变规律的叙述中不正确的是( )
| A、同主族元素从上到下,原子半径越大,金属性越强 |
| B、同周期元素从左到右(0族除外),非金属性逐渐增强 |
| C、同周期元素从左到右,气态氢化物稳定性逐渐增强 |
| D、同主族元素从上到下,原子半径越大,元素的第一电离能越大 |
设NA代表阿佛加德罗常数,下列说法正确的是( )
| A、22.4LCO和CO2的混和气体中所含的碳原子数一定是NA |
| B、标准状况下,22.4L氩气含有原子数为2NA |
| C、常温常压下,32gO2所含氧原子数为2NA |
| D、标准状况下,11.2LH2O含有0.5NA分子 |
往平底烧瓶中放入氢氧化钡晶体和氯化铵晶体,塞紧瓶塞.在木板上滴少量水,一会儿就会发现瓶内固态物质变成液体,瓶壁变冷,小木板上因少量水冻结,而被烧瓶粘住,这时打开瓶塞,出来的气体有氨味.这是自发地发生了反应:Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l),下列结论中正确的是( )
| A、自发反应一定是放热反 |
| B、自发反应一定是吸热反应 |
| C、有的吸热反应也能自发进行 |
| D、吸热反应不能自发进行 |
下列分子的空间构型可用sp3杂化轨道来解释的是( )
①PCl3 ②CH2═CH2 ③ ④CH≡CH⑤NH3 ⑥CH4.
④CH≡CH⑤NH3 ⑥CH4.
①PCl3 ②CH2═CH2 ③
 ④CH≡CH⑤NH3 ⑥CH4.
④CH≡CH⑤NH3 ⑥CH4.| A、①②③ | B、①⑤⑥ |
| C、②③④ | D、③⑤⑥ |