题目内容
依据题目要求回答下列问题.
(1)常温下,浓度均为 0.l mol?L-1的下列六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合H+ 能力最强的是
②根据表中数据,浓度均为0.0l mol?L-1的下列五种物质的溶液中,酸性最强的是 (填编号);将各溶液分别稀释100倍,pH变化最小的是 (填编号)
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是 (填编号)
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+NaClO=NaHCO3+HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为 .
(2)已知常温下Cu(OH)2的Ksp=2×10-20.又知常温下某CuSO4溶液里 c(Cu2+)2=0.02mol?L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于 .
(3)已知可逆反应FeO(s)+CO2(g)?Fe(s)+CO(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
①写出该反应平衡常数的表达式: .
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件:升高温度,混合气体的密度 (选填“增大”“减小”或“不变”);当
=0.5,混合气体平均相对分子质量为 .
(1)常温下,浓度均为 0.l mol?L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②根据表中数据,浓度均为0.0l mol?L-1的下列五种物质的溶液中,酸性最强的是
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+NaClO=NaHCO3+HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HC1O的浓度,可向氯水中加入少量的碳酸氢钠溶液,反应的离子方程式为
(2)已知常温下Cu(OH)2的Ksp=2×10-20.又知常温下某CuSO4溶液里 c(Cu2+)2=0.02mol?L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于
(3)已知可逆反应FeO(s)+CO2(g)?Fe(s)+CO(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
| T(K) | 938 | 1100 |
| K | 0.68 | 0.40 |
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件:升高温度,混合气体的密度
| n(CO2) |
| n(CO) |
考点:化学平衡的计算,盐类水解的原理,难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:(1)①酸的电离平衡常数越小,则酸的电离程度越小,酸根离子水解程度越大,相同浓度的钠盐溶液的pH越大,结合氢离子能力越大;
②酸的电离平衡常数越大,酸的电离程度越大,则酸的酸性越强,酸根离子水解程度越小,相同浓度的钠盐的PH越小;
加水稀释促进弱酸电离,相同浓度的不同酸稀释相同的倍数,酸的酸性越弱,酸的PH变化越小;
③根据强酸制取弱酸判断;
④HClO和碳酸氢钠不反应,盐酸和碳酸氢钠反应生成二氧化碳;
(2)根据Ksp=c(Cu2+)?[c(OH-)]2=2×10-20,根据Cu2+离子的浓度计算OH-离子的浓度,根据水的离子积常数计算氢离子浓度,并以此计算溶液pH值;
(3)①根据反应方程式FeO(s)+CO2(g)?Fe(s)+CO(g)书写K的表达式;
②根据影响化学平衡常数的因素进行分析,升温平衡常数减小,说明平衡逆向移动,正反应为放热反应.
②酸的电离平衡常数越大,酸的电离程度越大,则酸的酸性越强,酸根离子水解程度越小,相同浓度的钠盐的PH越小;
加水稀释促进弱酸电离,相同浓度的不同酸稀释相同的倍数,酸的酸性越弱,酸的PH变化越小;
③根据强酸制取弱酸判断;
④HClO和碳酸氢钠不反应,盐酸和碳酸氢钠反应生成二氧化碳;
(2)根据Ksp=c(Cu2+)?[c(OH-)]2=2×10-20,根据Cu2+离子的浓度计算OH-离子的浓度,根据水的离子积常数计算氢离子浓度,并以此计算溶液pH值;
(3)①根据反应方程式FeO(s)+CO2(g)?Fe(s)+CO(g)书写K的表达式;
②根据影响化学平衡常数的因素进行分析,升温平衡常数减小,说明平衡逆向移动,正反应为放热反应.
解答:
解:(1)①酸的电离平衡常数越小,则酸的电离程度越小,酸根离子水解程度越大,相同浓度的钠盐溶液的pH越大,结合氢离子能力越大,根据溶液的PH知,酸性最强的酸是醋酸,最弱的酸是碳酸氢根离子,则结合氢离子能力最大的是CO32-,故答案为:CO32-;
②酸的电离平衡常数越大,酸的电离程度越大,则酸的酸性越强,酸根离子水解程度越小,相同浓度的钠盐溶液的pH越小,所以酸性最强的是醋酸;
加水稀释促进弱酸电离,相同浓度的不同酸稀释相同的倍数,酸的酸性越弱,酸的PH变化越小,酸性最弱的酸是C6H5OH,则pH变化最小的是C6H5OH;
故答案为:D;C;
③A.醋酸酸性大于碳酸,所以CH3COOH+Na2CO3=NaHCO3+CH3COONa能发生,故不选;
B.醋酸酸性大于氢氰酸,所以CH3COOH+NaCN=CH3COONa+HCN能发生,故不选;
C.次氯酸酸性小于碳酸而大于碳酸氢根离子,所以CO2+H2O+NaClO=NaHCO3+HClO能发生,故不选;
D.碳酸酸性大于苯酚,所以CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH能发生,故选;
故答案为:D;
④HClO和碳酸氢钠不反应,盐酸和碳酸氢钠反应生成二氧化碳,所以导致氯水中HClO浓度增大,离子方程式为Cl2+HCO3-═CO2+Cl-+HClO;
故答案为:Cl2+HCO3-═CO2+Cl-+HClO;
(2)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,则应有c(OH-)≥
mol/L=10-9mol/L,则c(H+)≤
mol/L=10-5mol/L,
所以pH≥-lg(10-5)=5,故答案为:5;
(3)①根据反应方程式FeO(s)+CO2(g)?Fe(s)+CO(g)书写K,表达式为K=
,故答案为:K=
;
②升温平衡常数减小,说明平衡逆向移动,正反应为放热反应,气体体积不变,二氧化碳的摩尔质量大,所以混合气体的密度增大;
当
=0.5,K=
=2,n(CO):c(CO2)=2:1,混合气体平均相对分子质量为
=33.3.
故答案为:增大;33.3.
②酸的电离平衡常数越大,酸的电离程度越大,则酸的酸性越强,酸根离子水解程度越小,相同浓度的钠盐溶液的pH越小,所以酸性最强的是醋酸;
加水稀释促进弱酸电离,相同浓度的不同酸稀释相同的倍数,酸的酸性越弱,酸的PH变化越小,酸性最弱的酸是C6H5OH,则pH变化最小的是C6H5OH;
故答案为:D;C;
③A.醋酸酸性大于碳酸,所以CH3COOH+Na2CO3=NaHCO3+CH3COONa能发生,故不选;
B.醋酸酸性大于氢氰酸,所以CH3COOH+NaCN=CH3COONa+HCN能发生,故不选;
C.次氯酸酸性小于碳酸而大于碳酸氢根离子,所以CO2+H2O+NaClO=NaHCO3+HClO能发生,故不选;
D.碳酸酸性大于苯酚,所以CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH能发生,故选;
故答案为:D;
④HClO和碳酸氢钠不反应,盐酸和碳酸氢钠反应生成二氧化碳,所以导致氯水中HClO浓度增大,离子方程式为Cl2+HCO3-═CO2+Cl-+HClO;
故答案为:Cl2+HCO3-═CO2+Cl-+HClO;
(2)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,则应有c(OH-)≥
|
| 1×10-14 |
| 10-9 |
所以pH≥-lg(10-5)=5,故答案为:5;
(3)①根据反应方程式FeO(s)+CO2(g)?Fe(s)+CO(g)书写K,表达式为K=
| c(CO) |
| c(CO2) |
| c(CO) |
| c(CO2) |
②升温平衡常数减小,说明平衡逆向移动,正反应为放热反应,气体体积不变,二氧化碳的摩尔质量大,所以混合气体的密度增大;
当
| n(CO2) |
| n(CO) |
| c(CO) |
| c(CO2) |
| 28×2+44 |
| 2+1 |
故答案为:增大;33.3.
点评:本题考查了平衡常数,盐类水解,溶度积常数的计算,题目综合性较强,难度不大,注意把握计算公式的运用、H2CO3、HClO、HCO3-酸性强弱关系.

练习册系列答案
相关题目
同条件等体积等pH的醋酸和盐酸分别加水稀释后,溶液的pH仍相同,则所得溶液的体积( )
| A、仍相同 | B、醋酸大 |
| C、盐酸大 | D、无法判断 |
水是人类不可缺少的物质,学校为了师生的饮水方便,投入大量资金购置了直饮水机,有关这类直饮水的下列说法中,正确的是( )
| A、它是纯天然饮品,不含任何化学物质 |
| B、它清洁、纯净,但长期饮用对健康无益 |
| C、它含有人体所需的矿物质和多种微量元素 |
| D、用催化剂可将它转化为汽油 |
胡椒酚是植物挥发油的成分之一,它的结构简式为:HO- -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )
 -CH2CH=CH2,下列叙述中正确的是( )
-CH2CH=CH2,下列叙述中正确的是( )| A、1mol胡椒酚最多可与4molH2发生反应 |
| B、1mol胡椒酚最多可与4mol溴发生反应 |
| C、胡椒酚中所有原子可以共平面 |
| D、胡椒酚在水中的溶解度小于苯酚在水中的溶解度 |
设C+CO2═2CO(正反应吸热),该反应速率v1;N2+3H2?2NH3(正反应放热),该反应速率v2.若升温,v1和v2的变化是( )
| A、同时增大 |
| B、同时减少 |
| C、v1增大,v2减少 |
| D、v1减少,v2增大 |
下列说法正确的是( )
| A、石墨比金刚石稳定,故石墨转化为金刚石的反应可以自发进行 |
| B、吸热反应能自发进行的原因是从外界获得了能量 |
| C、Si02常温下可以与NaOH溶液和HF溶液反应,说明其具有两性 |
| D、反应A(g)+B(g)=2C(s)可以自发进行,则其必为放热反应 |
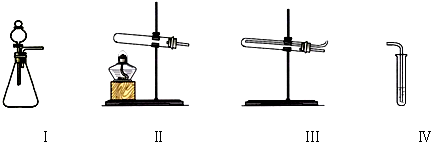
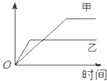 表格中的各种情况,可以用如图的曲线表示的是( )
表格中的各种情况,可以用如图的曲线表示的是( )