题目内容
8.将CH4设计成燃料电池,装置如图所示(A、B为多孔碳棒)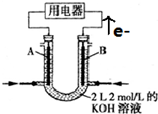
(1)B(填A或B)处电极入口通甲烷,其电极反应式为CH4+10OH--8e-═CO32-+7H2O;
(2)当消耗甲烷的体积为11.2L(标准状况下)时,则导线中转移电子的物质的量为4mol,消耗KOH的质量为56g.
分析 (1)根据电子流向知,A为负极、B为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,甲烷失电子和氢氧根离子反应生成碳酸根离子和水;
(2)根据甲烷和转移电子、氢氧化钾之间的关系式计算.
解答 解:(1)根据电子流向知,B为负极、A为正极,燃料电池中通入燃料的电极为负极、通入氧化剂的电极为正极,所以B处通入甲烷,甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH4-8e-+10OH-═CO32-+7H2O,故答案为:B;CH4-8e-+10OH-═CO32-+7H2O;
(2)甲烷的物质的量为0.5mol,导线中转移电子的物质的量=0.5mol×8=4mol,根据CH4-8e-+10OH-═CO32-+7H2O知,消耗KOH的物质的量为甲烷物质的量的10倍,所以消耗氢氧化钾的物质的量是1mol,质量是56g,
故答案为:4 mol;56g.
点评 本题考查了原电池和电解池原理,根据元素化合价变化确定氧化性强弱,根据方程式中各个物理量之间的关系式进行计算,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
19.下列关于卤素(氟氯溴碘元素,简称为卤素)的叙述正确的是( )
①卤素的钾盐中,所有卤素的化合价均为-1价
②溴中溶有少量氯气,可以用加入溴化钠再用苯萃取的方法提纯
③溴化银具有感光性,碘化银不具有感光性
④某溶液与淀粉KI溶液混合后出现蓝色,则证明该溶液是氯水或溴水
⑤氯气与水溶液反应,一定有酸生成⑥氯气跟水反应时,水既不作氧化剂也不是还原剂.
①卤素的钾盐中,所有卤素的化合价均为-1价
②溴中溶有少量氯气,可以用加入溴化钠再用苯萃取的方法提纯
③溴化银具有感光性,碘化银不具有感光性
④某溶液与淀粉KI溶液混合后出现蓝色,则证明该溶液是氯水或溴水
⑤氯气与水溶液反应,一定有酸生成⑥氯气跟水反应时,水既不作氧化剂也不是还原剂.
| A. | ①③⑤ | B. | ②③⑥ | C. | ②⑤⑥ | D. | ①③④ |
16.物质的量浓度相同的下列溶液中,符合按pH由小到大排列的是( )
| A. | Na2CO3 NaHCO3 NaCl NH4Cl | |
| B. | Na2CO3 NaHCO3 NH4Cl NaCl | |
| C. | (NH4)2SO4 NH4Cl NaNO3 Na2S | |
| D. | NH4Cl (NH4)2SO4 Na2S NaNO3 |
13.下列4个有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH3CH2CH2OH ④CH2=CHCH2OH⑤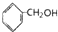
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH3CH2CH2OH ④CH2=CHCH2OH⑤

| A. | ①③ | B. | ①④⑤ | C. | ②④ | D. | ①②③⑤ |
20.对于放热反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,下列说法正确的是( )
| A. | H2与Cl2混合后点燃与 H2 在Cl2中安静燃烧的反应速率是一样大的 | |
| B. | 反应物所具有的总能量高于产物所具有的总能量 | |
| C. | 断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成1mol H-Cl键所放出的能量 | |
| D. | 该反应中,化学能只转变为热能 |
17.下列推断正确的是( )
| A. | 常温下硅性质活泼,可以与氯气、强酸、强碱溶液等起反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
18.A、B、C为三种短周期元素,A、B在同周期,A、C的最低价离子分别为A2-和C-.B2+和C-具有相同的电子层结构.下列说法中,正确的是( )
| A. | 原子序数B>A>C | B. | 原子半径A>B>C | ||
| C. | 离子半径A2->B2+>C- | D. | 原子最外层电子数C>A>B |