题目内容
3.研究含氮、碳化合物的性质对它们的综合利用有重要意义.(1)反应NO+O3=NO2+O2,若生成11.2L O2(标准状况)时,转移电子的物质的量是1mol
(2)硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g)?SO3(g)+NO(g)△H=-41.8kJ•mol-1
已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
写出NO和O2反应生成NO2的热化学方程式2NO(g)+O2(g)=2NO2(g)△H=-113.0 kJ•mol-1
(3)N2H4(肼或联氨)燃料电池(产生稳定、无污染的物质)原理如图1所示.M电极发生的电极反应式
为N2H4-4e-=N2↑+4H+
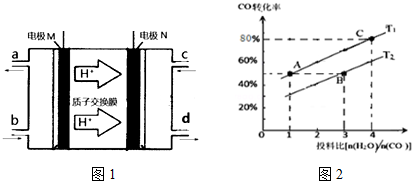
(4)已知CO (g)+H2O (g)?H2 (g)+CO2 (g)△H>0
①一定条件下反应达到平衡状态后,若改变反应的某个条件,下列变化能说明平衡一定向正反应方向移动的是C(填写字母)
A.逆反应速率先增大后减小 B.H2O (g)的体积百分含量减小
C.CO的转化率增大 D.容器中$\frac{c(C{O}_{2})}{c(CO)}$的值减小
②在某压强下,上述反应在不同温度、不同投料比时,CO的转化率如图2所示.则KA、KB、KC三者之间的大小关系为KA=KC>KB.
T1温度下,将1molCO和4mol H2O (g)充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CO)=0.08mol•L-1•min-1;若保持其他条件不变,向平衡体系中再通入1molCO和1molCO2,此时v(正)>v(逆)(填“>”、“=”或“<”)
分析 (1)化合价升高值=化合价降低值=转移电子数,根据化合价的变化来确定电子转移数目;
(2)A、NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-41.8kJ•mol-1;B、2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1,则反应:2NO(g)+O2(g)=2NO2(g)可以看成是B-2A得到的,根据盖斯定律结合热化学方程式的书写来回答;
(3)由氢离子的移动方向可知,M区为负极,发生失电子的氧化反应;
(4)①A.逆反应速率先增大后减小,可能是增大生成物浓度;
B.H2的转化率增大,平衡一定正向移动;
C.反应物的体积百分含量减小,可能是增大生成物浓度等;
D.容器中的二氧化碳和氢气浓度比值变小,可能是减小二氧化碳的物质的量.
②根据平衡常数仅与温度有关,温度不变,平衡常数不变,T1温度下,根据平均反应速率v(CO)=$\frac{△c}{△t}$来计算,根据Qc和K的关系判断反应的方向.
解答 解:(1)NO+O3═NO2+O2,生成1mol氧气转移电子是2mol,生成11.2L即0.5mol O2(标准状况)时,转移电子的物质的量是1mol,故答案为:1;
(2)已知:A、NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-41.8kJ•mol-1;
B、2SO2(g)+O2(g)=2SO3(g)△H=-196.6kJ•mol-1,则反应:2NO(g)+O2(g)=2NO2(g)可以看成是B-2A得到的,所以该反应的△H=-196.6kJ•mol-1-2(-41.8kJ•mol-1)=-113.0 kJ•mol-1,故答案为:2NO(g)+O2(g)=2NO2(g)△H=-113.0 kJ•mol-1;
(3)由氢离子的移动方向可知,M区为负极,发生的电极反应式为N2H4-4e-=N2↑+4H+,故答案为:N2H4-4e-=N2↑+4H+;
(4)①A.逆反应速率先增大后减小,可能是增大生成物浓度,平衡逆向移动,故A错误;
B.H2O(g)的体积百分含量减小,可能是增大生成物浓度,平衡不一定正向移动,故B错误;
C.CO的转化率增大,平衡正向移动,故C正确;
D.容器中的二氧化碳和氢气浓度比值变小,可能是减小二氧化碳的物质的量,平衡逆向移动,故D错误,
故选:C;
②平衡常数仅与温度有关,温度不变,平衡常数不变,所以KA=KC,反应是吸热反应,所以升高温度,平衡正向移动,CO的转化率增加,T2<T1,温度越高,K越大,所以KA=KC>KB,T1温度下,将1molCO和4mol H2O (g)充入2L的密闭容器中,5min后反应达到平衡状态,此时CO的转化率是80%,则0~5min内的平均反应速率v(CO)=$\frac{\frac{1mol}{2L}×80%}{5min}$=0.08mol•L-1•min-1,CO的平衡浓度是0.1mol/L,H2O(g)的平衡浓度是1.6mol/L,H2、CO2 的平衡浓度是0.4mol/L,
此时K=$\frac{0.4×0.4}{0.1×1.6}$=1,若保持其他条件不变,向平衡体系中再通入1molCO和1molCO2,此时Qc=$\frac{0.4×0.9}{0.6×1.6}$<1,即Qc<K,所以v(正)>v(逆),
故答案为:0.08mol•L-1•min-1;>.
点评 本题考查化学平衡计算与影响因素、盖斯定律的应用、对图象分析提取信息能力等,较好的考查学生对知识的迁移应用.

 阅读快车系列答案
阅读快车系列答案| A. | 稀盐酸 | B. | 硫酸铜溶液 | C. | 酒精 | D. | 氯化钠(熔融) |
| A. | 变性蛋白质不能食用 | |
| B. | 可用甲醛浸泡海鲜 | |
| C. | SO2可以用来增白食品 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂 |
| 元素代号 | X | Y | Z | M | Q | R |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.037 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
| A. | Z、Q均为ⅣA族元素 | |
| B. | X、Y、M三种元素中金属性最强的是M | |
| C. | R、Z形成的R2Z分子是非极性分子 | |
| D. | M的氢氧化物和Y的氢氧化物都能与氢氧化钠溶液反应 |
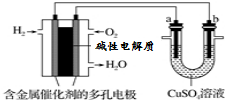
| A. | 此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 | |
| B. | 若a为纯铜,b为粗铜,该装置可用于粗铜的电解精炼 | |
| C. | 燃料电池中正极反应为O2+4e-+2H2O=4OH- | |
| D. | 电子经导线流入b电极 |

| A. | X与Y组成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | W、R两种元素对应的简单离子都能影响水的电离平衡 | |
| C. | 由X、Y、Z三种元素组成的化合物,其水溶液显碱性 | |
| D. | 工业上用电解熔融的Z和X组成的化合物来制取Z的单质 |
| A. | 葡萄糖和蛋白质等高分子化合物是人体必需的营养物质 | |
| B. | 自来水厂用明矾净水,也可以用ClO2代替 | |
| C. | 居室中放置一盆石灰水可以吸收CO,预防中毒 | |
| D. | 用二氧化碳生产聚碳酸酯可以减少碳排放,以减缓温室效应 |
 海水中主要离子的含量如下:
海水中主要离子的含量如下:| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
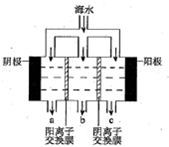
(2)电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.阴极上产生氢气,阴极附近还产生少量白色沉淀,其成分有Mg(OH)2和CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O.
(3)用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:
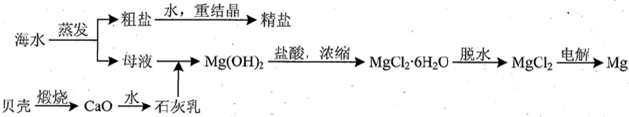
①在实验室中由粗盐“重结晶”制精盐的操作包括溶解、过滤、蒸发…洗涤等步骤;有关其中“蒸发”步骤的叙述正确的是bd.
a.蒸发的目的是得到热饱和溶液
b.蒸发的目的是析出晶体
c.应用余热蒸干溶液
d.应蒸发至有较多晶体析出时为止
②由MgCl2溶液得到MgCl2•6H2O晶体时,也需要蒸发,蒸发的目的是得到热饱和溶液,判断溶液已饱和的现象是溶液表面形成晶膜.
(4)25℃时,饱和Mg(OH)2溶液的浓度为5×10-4 mol/L.
①饱和Mg(OH)2溶液中滴加酚酞,现象是溶液变红.
②某学习小组测海水中Mg2+含量(mg/L)的方法是:取一定体积的海水,加入足量盐酸,再加入足量NaOH,将Mg2+转为Mg(OH)2.25℃,该方法测得的Mg2+含量与表中1272mg/L的“真值”比,相对误差约为-5.6%[保留2位小数,海水中饱和Mg(OH)2溶液的密度都以l g/cm3计].
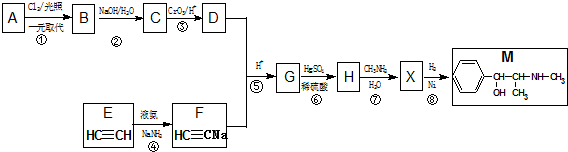
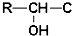 ≡C-R′
≡C-R′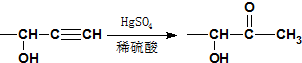
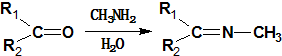
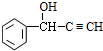 .
. +CH3NH2$\stackrel{水}{→}$
+CH3NH2$\stackrel{水}{→}$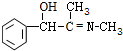 +H2O.
+H2O.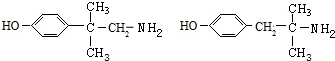 (任写一种).
(任写一种).