题目内容
如图,甲、乙、丙分别表示在不同条件下可逆反应A(g)+B(g)?xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系.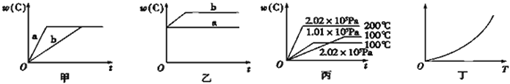
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下充入氦气后的情况,则
(3)根据丙图可以判断该可逆反应的正反应是
(4)丁图表示在某固定容积的密闭容器中上述可逆反应达到平衡后某物理量随着温度(T)的变化情况,根据你的理解,丁图的纵坐标可以是
分析:(1)使用催化剂,加快反应速率,缩短到达平衡的时间,据此判断;
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,据此解答.
(4)根据(3)中可知该反应为吸热反应还是放热反应,升高温度,平衡向吸热方向移动.由图可知,纵轴所表示的量随温度升高而增大,根据平衡移动分析.
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,据此解答.
(4)根据(3)中可知该反应为吸热反应还是放热反应,升高温度,平衡向吸热方向移动.由图可知,纵轴所表示的量随温度升高而增大,根据平衡移动分析.
解答:解:(1)使用催化剂,加快反应速率,缩短到达平衡的时间,由图可知,a先到达平衡,故a曲线表示使用催化剂,b曲线表示没有使用催化剂,故答案为:b;
b达到平衡用到的时间长,化学反应速率慢,没有使用催化剂;
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动,C%不变,故答案为:a;A中充入氦气,w(C)不变,平衡不移动;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,正反应为吸热反应,温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,故x>1+1,即x>2,
故答案为:吸;x>2;
(4)该反应正反应为吸热反应,反应前后气体的体积增大.升高温度,平衡向吸热方向移动,即向右移动.由图可知,纵轴所表示的量随温度升高而增大,升高温度,平衡向吸热方向移动,即向右移动,C的含量增大,A、B的转化率增大,平衡时A、B浓度降低.反应前后气体的体积增大,在恒容条件下,升高温度,平衡向吸热方向移动,即向右移动,混合物总的物质的量增加,所以平衡时,容器内压强增大,故答案为:C%;A的转化率(或是B的转化率、压强).
b达到平衡用到的时间长,化学反应速率慢,没有使用催化剂;
(2)恒温恒容条件下,通入惰性气体,不影响反应混合气体各组分的浓度,平衡不移动,C%不变,故答案为:a;A中充入氦气,w(C)不变,平衡不移动;
(3)由丙图可知,相同压强温度越高,C%越大,说明升高温度,平衡向正反应移动,正反应为吸热反应,温度相同压强越高,C%越小,说明增大压强,平衡向逆反应移动,故x>1+1,即x>2,
故答案为:吸;x>2;
(4)该反应正反应为吸热反应,反应前后气体的体积增大.升高温度,平衡向吸热方向移动,即向右移动.由图可知,纵轴所表示的量随温度升高而增大,升高温度,平衡向吸热方向移动,即向右移动,C的含量增大,A、B的转化率增大,平衡时A、B浓度降低.反应前后气体的体积增大,在恒容条件下,升高温度,平衡向吸热方向移动,即向右移动,混合物总的物质的量增加,所以平衡时,容器内压强增大,故答案为:C%;A的转化率(或是B的转化率、压强).
点评:本题考查化学平衡图象、影响化学平衡的因素,难度中等,注意分析图象中曲线的变化特点,结合平衡移动原理解答.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目


 xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。下列说法与图像符合的是
xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。下列说法与图像符合的是
 xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。下列说法与图像符合的是
xC(g)的生成物C在反应混合物中的百分含量w(C)和反应时间(t)的关系。下列说法与图像符合的是


