题目内容
5.含1molAlCl3的溶液中滴加NaOH溶液,充分反应后生成沉淀39g,求加入NaOH的物质的量?分析 1molAlCl3完全转化为氢氧化铝沉淀的质量为1mol×78g/mol=78g,根据Al3++3OH-=Al(OH)3↓和Al(OH)3+OH-=AlO2-+H2O,可知NaOH存在两种情况,一是不足,二是使Al(OH)3部分溶解,以此解答该题.
解答 解:1molAlCl3完全转化为氢氧化铝沉淀的质量为1mol×78g/mol=78g,根据Al3++3OH-=Al(OH)3↓和Al(OH)3+OH-=AlO2-+H2O,可知NaOH存在两种情况,一是不足,二是使Al(OH)3部分溶解,
当NaOH不足时,
Al3++3OH-=Al(OH)3↓
3mol 78g
x 39g
x=1.5mol,
当NaOH使Al(OH)3部分溶解时,设NaOH的物质的量为y,根据反应:
Al3++3OH-=Al(OH)3↓
1mol 3mol 78g
Al(OH)3 +OH-=AlO2-+H2O
78g 1mol
(78-39)g (y-3mol)
y=3.5mol,
答:加入NaOH的物质的量可能为1.5mol、3.5mol.
点评 本题考查化学方程式的计算,为高频考点,侧重考查学生的分析、计算能力,注意掌握氢氧化铝的两性和判断氯化铝反应的程度为解答本题的关键,用讨论法解答,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列有关硅元素、氯元素的单质及其化合物的说法错误的是( )
①在常温下,硅的化学性质很活泼
②氯气能与所有金属化合,生成金属氯化物
③硅酸钠可以用来制备硅胶和木材防火剂
④漂粉精的主要成分是次氯酸钙和氯化钙.
①在常温下,硅的化学性质很活泼
②氯气能与所有金属化合,生成金属氯化物
③硅酸钠可以用来制备硅胶和木材防火剂
④漂粉精的主要成分是次氯酸钙和氯化钙.
| A. | ①③④ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
20.取9.20g铜和镁的合金完全溶于某硝酸溶液,反应中产生8 960mL NO2气体和448mL NO气体(已折算成标准状况).向反应后的溶液中加入足量的氢氧化钠溶液,则生成沉淀的质量为( )
| A. | 11.24 g | B. | 22.8 g | C. | 17.02 g | D. | 24.84 g |
10.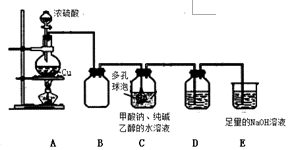 已知:①、连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇.②4HCl+2Na2S2O4═4NaCl+S↓+3SO2↑+2H2O某小组进行如下实验:
已知:①、连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇.②4HCl+2Na2S2O4═4NaCl+S↓+3SO2↑+2H2O某小组进行如下实验:
I.制备:75℃时,将甲酸钠和纯碱加入乙醇水溶液溶解后,再加入装置 C 中,然后通入 SO2进行反应,其反应方程式为:2HCOONa+Na2CO3+4SO2═2Na2S2O4+3CO2+H2O.
分析并回答下列问题:
(1)装置(图)A中滴加浓硫酸的仪器名称是分液漏斗,A 中反应的化学方程式为Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;冷却至 40~50℃,过滤,用乙醇洗涤,干燥制得 Na2S2O4.
(2)C 中多孔球泡的作用是增大接触面积,促进SO2的吸收
(3)装置 D的作用是检验装置 C中 SO2的吸收效率,D中的试剂可以是cd
a.酚酞溶液 b.氢氧化钠溶液 c.品红溶液 d.酸性KMnO4溶液
(4)装置E的作用吸收尾气
II.Na2S2O4 的性质】
取纯净的 Na2S2O4晶体,配成溶液,进行下列性质探究实验,完成表的空格(供选择的试剂:淀粉-KI 溶液、紫色石蕊试液、稀硝酸、BaCl2 溶液)
III.【测定 Na2S2O4 的纯度】
取 8.00g制备的晶体溶解后,加入足量稀硫酸,充分反应后,过滤、洗涤、干燥.得固体 0.64g.则 Na2S2O4 的纯度为87%[已知:M(Na2S2O4)=174.0].
 已知:①、连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇.②4HCl+2Na2S2O4═4NaCl+S↓+3SO2↑+2H2O某小组进行如下实验:
已知:①、连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇.②4HCl+2Na2S2O4═4NaCl+S↓+3SO2↑+2H2O某小组进行如下实验:I.制备:75℃时,将甲酸钠和纯碱加入乙醇水溶液溶解后,再加入装置 C 中,然后通入 SO2进行反应,其反应方程式为:2HCOONa+Na2CO3+4SO2═2Na2S2O4+3CO2+H2O.
分析并回答下列问题:
(1)装置(图)A中滴加浓硫酸的仪器名称是分液漏斗,A 中反应的化学方程式为Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;冷却至 40~50℃,过滤,用乙醇洗涤,干燥制得 Na2S2O4.
(2)C 中多孔球泡的作用是增大接触面积,促进SO2的吸收
(3)装置 D的作用是检验装置 C中 SO2的吸收效率,D中的试剂可以是cd
a.酚酞溶液 b.氢氧化钠溶液 c.品红溶液 d.酸性KMnO4溶液
(4)装置E的作用吸收尾气
II.Na2S2O4 的性质】
取纯净的 Na2S2O4晶体,配成溶液,进行下列性质探究实验,完成表的空格(供选择的试剂:淀粉-KI 溶液、紫色石蕊试液、稀硝酸、BaCl2 溶液)
| 假设 | 操作 | 现象 | 原理 |
| Na2S2O4 为强 碱弱酸盐,其溶 液为碱性. | 取少量溶液于试管中, 滴加紫色水蕊试液 | 溶液变 成蓝色 | S2O42-水解,使溶液成碱性 |
| Na2S2O4 中 S为+3 价,具有较强 的还原性. | 取少量溶液于试管中, 滴加过量新制氯水,再 滴加 BaCl2 溶 | 有白色沉淀生 成 | 该反应的离子方程式为:4H2O+S2O42-+3Cl2=2SO42-+6Cl-+8H+ ,Ba2++SO42-=BaSO4↓; |
取 8.00g制备的晶体溶解后,加入足量稀硫酸,充分反应后,过滤、洗涤、干燥.得固体 0.64g.则 Na2S2O4 的纯度为87%[已知:M(Na2S2O4)=174.0].
17.向50.0mL未知浓度的HCl溶液中加入一定质量分数为20%的AgNO3溶液,充分反应后盐酸有剩余,再向溶液中滴加20g质量分数为20%的NaOH溶液恰好完全反应,则原HCl溶液物质的量浓度是( )
| A. | 1.0mol•L-1 | B. | 2.0mol•L-1 | C. | 4.0mol•L-1 | D. | 无法计算 |
14.如图所示是几种常见的化学电源示意图,有关说法不正确的是( )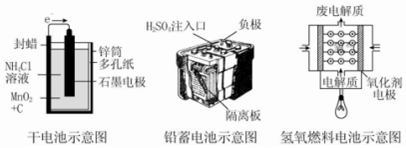

| A. | 上述电池分别属于一次电池、二次电池和燃料电池 | |
| B. | 干电池在长时间使用后,锌筒被破坏 | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 铅蓄电池工作过程中,每通过 2 mol 电子,负极质量减轻 207 g |
15.下列反应可用离子方程式“H++OH-=H2O”表示的是( )
| A. | NaHSO4溶液与Ba(OH)2溶液混合 | B. | NH4Cl溶液与Ca(OH)2溶液混合 | ||
| C. | HNO3溶液与KOH溶液混合 | D. | CH3COOH溶液与NaOH溶液混合 |