题目内容
19.下列有关物质转化关系的说法中不正确的是( )| A. | 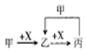 图中甲可能是Cl2,X可能是Fe | |
| B. |  图中反应一定是置换反应或复分解反应 | |
| C. | 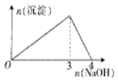 图中是向某溶液中滴加NaOH溶液的变化图象,原溶质可能是Al2(SO4)3 | |
| D. | 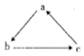 图中a可能为NaOH,b可能为Na2CO3,c可能为NaHCO3 |
分析 A、铁和氯气反应生成氯化铁,氯化铁在溶液中和铁反应生成氯化亚铁,氯气能把氯化亚铁氧化为氯化铁;
B、根据置换反应或复分解反应的概念进行判断;
C、向硫酸铝溶液中逐滴加入氢氧化钠溶液的方程式为Al3++3OH-=Al(OH)3↓,氢氧化钠过量后发生反应Al(OH)3+OH-=AlO2-+2H2O;
D、氢氧化钠溶液中通入少量CO2生成 碳酸钠和H2O,向碳酸钠溶液中继续通入CO2生成碳酸氢钠,碳酸氢钠和盐酸反应转化为CO2.
解答 解:A、铁和氯气反应生成氯化铁,氯化铁在溶液中和铁反应生成氯化亚铁,氯气能把氯化亚铁氧化为氯化铁,则甲可能是Cl2,X可能是Fe,故A正确;
B、图中反应不一定是置换反应或复分解反应,例如在加热的条件下CO与氧化铜反应生成铜和CO2也符合图中转换,故B错误;
C、向硫酸铝溶液中逐滴加入氢氧化钠溶液的方程式为Al3++3OH-=Al(OH)3↓,氢氧化钠过量后发生反应Al(OH)3+OH-=AlO2-+2H2O,则图象正确,故C正确;
D、向氢氧化钠溶液中通入少量CO2生成 碳酸钠和H2O,向碳酸钠溶液中继续通入CO2生成碳酸氢钠,碳酸氢钠和盐酸反应转化为CO2,所以a可能为NaOH,b可能为Na2CO3,c可能为NaHCO3,故D正确;
故选:B.
点评 本题考查了常见物质的性质及相互间的反应,熟练掌握酸碱盐等物质的化学性质,并能根据反应物的种类来判断反应的情况是解题的关键所在.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列化学实验对应的现象及结论都正确且两者具有因果关系的是( )
| 实验 | 现象 | 结论 | |
| A | 向浓度均为0.1mol/L的NaHCO3溶液和NaHSO3溶液中滴加几滴酚酞试剂 | 前者溶液变红,后者不变色 | NaHCO3水解,而NaHSO3不水解 |
| B | 向NaAlO2溶液中通入NH3 | 白色沉淀 | Al(OH)3不能溶解在弱碱中 |
| C | 向滴有品红的水中通入SO2 | 溶液红色褪去 | SO2具有氧化性 |
| D | 将充有NO2的密闭烧瓶放入热水中 | 烧瓶内气体颜色变深 | NO2生成N2O4的反应中,△H<0 |
| A. | A | B. | B | C. | C | D. | D |
10.下列分子式表示的物质,没有同分异构体的是( )
| A. | C4H10 | B. | C3H8 | C. | C4H8 | D. | C5H12 |
7. 过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:
过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:
(1)H2O2的电子式为 .
.
(2)用H2O2与稀硫酸的混合溶液可溶出印刷电路板金属粉末中的铜.
已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ/mol
2H2O2(1)═2H2O(l)+O2(g)△H=-196kJmol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol
则在稀硫酸溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol.
(3)工业上常用电解硫酸氢铵水溶液的方法制备过氧化氢,其原理为:首先2NH4HSO4$\frac{\underline{\;通电\;}}{\;}$(NH4)2S2O8+H2↑,然后由(NH4)2S2O8水解得到H2O2和另一产物.则:
①电解时阳极的电极反应式为2SO42--2e-=S2O82-;
②(NH4)2S2O8水解时发生反应的化学方程式为(NH4)2S2O8+2H2O=2NH4HSO4+H2O2.
(4)现甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变).甲小组有如下实验设计方案.
甲、乙两小组得出如图数据.
①甲小组实验得出的结论是H2O2分解时,MnO2比Fe2O3催化效率更高.
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析,相同条件下H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2固体与硫酸溶液反应制H2O2,其反应的离子方程式为BaO2+2H++SO42-═BaSO4↓+H2O2;支持这一方案的理由是(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性环境有利于H2O2的存在(等其他合理原因).
③已知过氧化氢还是一种极弱的二元酸:H2O2?H++HO2-(K${\;}_{{a}_{1}}$=2.4×10-12).当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH-?HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)•c(OH-),逆反应速率为v逆=k逆•c(H2O)•c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为1.33×104(保留3位有效数字).
 过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:
过氧化氢(H2O2)俗称双氧水.是一种重要的化工产品,具有漂白、氧化、消毒、杀菌等多种功效,广泛应用于纺织、造纸、化工、电子、轻工、污水处理等工业.回答下列问题:(1)H2O2的电子式为
 .
.(2)用H2O2与稀硫酸的混合溶液可溶出印刷电路板金属粉末中的铜.
已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64kJ/mol
2H2O2(1)═2H2O(l)+O2(g)△H=-196kJmol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol
则在稀硫酸溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=-320kJ/mol.
(3)工业上常用电解硫酸氢铵水溶液的方法制备过氧化氢,其原理为:首先2NH4HSO4$\frac{\underline{\;通电\;}}{\;}$(NH4)2S2O8+H2↑,然后由(NH4)2S2O8水解得到H2O2和另一产物.则:
①电解时阳极的电极反应式为2SO42--2e-=S2O82-;
②(NH4)2S2O8水解时发生反应的化学方程式为(NH4)2S2O8+2H2O=2NH4HSO4+H2O2.
(4)现甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时间长短来探究影响H2O2分解速率的因素(仅一个条件改变).甲小组有如下实验设计方案.
| 实验编号 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 25℃ | 三氧化二铁 | 10mL5%H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2 |
①甲小组实验得出的结论是H2O2分解时,MnO2比Fe2O3催化效率更高.
②由乙组研究的酸、碱对H2O2分解影响因素的数据分析,相同条件下H2O2在碱(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2固体与硫酸溶液反应制H2O2,其反应的离子方程式为BaO2+2H++SO42-═BaSO4↓+H2O2;支持这一方案的理由是(BaSO4的生成有利于平衡右移即有利于H2O2的生成)酸性环境有利于H2O2的存在(等其他合理原因).
③已知过氧化氢还是一种极弱的二元酸:H2O2?H++HO2-(K${\;}_{{a}_{1}}$=2.4×10-12).当稀H2O2溶液在碱性环境下分解时会发生反应H2O2+OH-?HO2-+H2O,该反应中,正反应速率为V正=k正•c(H2O2)•c(OH-),逆反应速率为v逆=k逆•c(H2O)•c(HO2-),其中k正、k逆为速率常数,则k正与k逆的比值为1.33×104(保留3位有效数字).
14.化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A. | “滴水石穿、绳锯木断”涉及到化学变化 | |
| B. | 乙酸乙酯在H218O中水解,产物乙醇中将含有18O同位素 | |
| C. | 氟利昂作制冷剂会加剧雾霾天气的形成 | |
| D. | 汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的 |
4.化学与生产、生活密切相关,下列有关说法不正确的是( )
| A. | 水玻璃是用于生产硅胶、木材防火剂、粘合剂的原料 | |
| B. | 可以用氢氧化钠溶液鉴别地沟油和矿物油 | |
| C. | CaCO3分解,Ba(OH)2•8H2O和NH4Cl 反应,高温下铝与氧化铁的反应都是吸热反应 | |
| D. | 淀粉、蛋白质、有机玻璃、天然橡胶都是高分子化合物 |
11.下列实验能达到相应目的是( )
| 选项 | A | B | C | D |
| 实验 过程 |  |  |  |  |
| 实验 目的 | 将乙二醇(HOCH2CH2OH)转化为乙二酸(H2C2O4) | 比较氯化铁和二氧化锰对H2O2分解反应的催化效果 | 证明稀硝酸与铜反应时表现出氧化性 | 用SO2与Ba(NO3)2反应获得BaSO3沉淀 |
| A. | A | B. | B | C. | C | D. | D |
8.化学与生活、生产紧密相关,对下列现象或事实的解释正确的选项是( )
| 选项 | 现象或事实 | 解释 |
| A | 用热的烧碱溶液洗涤餐具 | NaOH能使油脂发生水解反应 |
| B | 向普通钢材中添加少量镍、铬等其它金属 | 形成合金,保护铁不被腐蚀 |
| C | 处理锅炉内壁的水垢需使用Na2CO3溶液 | 将Mg(OH)2转化为更难溶的MgCO3 |
| D | 使用明矾净水 | 明矾溶液显酸性 |
| A. | A | B. | B | C. | C | D. | D |