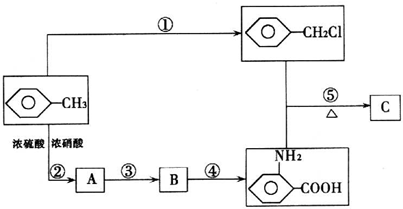
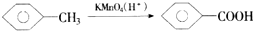题目内容
氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A、10mL 1mol/HCN恰好与10mL 1mol/LNaOH溶液完全反应 |
| B、1mol/L HCN溶液的pH约为3 |
| C、在相同条件下,HCN溶液的导电性比强酸溶液的弱 |
| D、HCN易溶于水 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氢氰酸为弱电解质,则利用其电离不完全来分析,一般测定溶液的pH或测定相同条件下与强酸的导电性比较以及对应盐溶液的酸碱性来判断.
解答:
解:A.二者物质的量相等,不能证明酸性的强弱,故A错误;
B.氢氰酸为一元酸,1mol/L氢氰酸溶液的pH=0时该酸为强酸,但pH约为3,说明电离生成的氢离子约为10-3mol/L<1mol/L,电离不完全,故B正确;
C.相同条件下,氢氰酸溶液的导电性比强酸溶液的弱,不知道强酸是几元酸,不能能说明氢氰酸电离不完全,故C错误;
D.不能利用物质的溶解性来判断是否为弱电解质,即溶解性与电解质的强弱无关,故D错误;
故选B.
B.氢氰酸为一元酸,1mol/L氢氰酸溶液的pH=0时该酸为强酸,但pH约为3,说明电离生成的氢离子约为10-3mol/L<1mol/L,电离不完全,故B正确;
C.相同条件下,氢氰酸溶液的导电性比强酸溶液的弱,不知道强酸是几元酸,不能能说明氢氰酸电离不完全,故C错误;
D.不能利用物质的溶解性来判断是否为弱电解质,即溶解性与电解质的强弱无关,故D错误;
故选B.
点评:本题考查弱电解质的判断方法,明确弱电解质在水中电离不完全是解答本题的关键,学生应注意在平时的学习中归纳判断弱电解质的方法,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
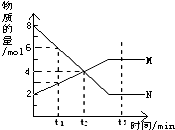 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2N?M |
| B、Bt2时,正逆反应速率相等,达到平衡 |
| C、t1时,N的浓度是M的浓度的2倍 |
| D、t3时,正反应速率大于逆反应速率 |
常温下,下列电解质溶液的有关叙述正确的是( )
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| C、pH═11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| D、同浓度同体积的强酸与强碱溶液混合后,溶液的pH=7 |
下列电解质溶液的有关叙述正确的是( )
| A、在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
| B、pH=3的CH3COOH与pH=11的NaOH溶液等体积混合后,溶液显碱性 |
| C、将足量CuSO4溶液在0.1mol?L-1的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol?L-1(已知:Ksp(CuS)=1.3×10-36) |
| D、含1molKOH的溶液与1molCO2完全反应后,溶液中c(K+)=c(HCO3-) |
100mL浓度为2mol/L的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气总量,可采用的方法是( )
| A、加入少量浓盐酸 |
| B、加入几滴氯化铜溶液 |
| C、加入少量铁粉 |
| D、加入适量的氯化钠溶液 |