题目内容
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
| A、含4 mol Si-O键的二氧化硅晶体中,氧原子数为2NA |
| B、1.8 g重水(D2O)中含有的质子数和电子数均为NA |
| C、1 L 1mol?L-1的CH3COONa溶液中含有CH3COO-的数目为NA |
| D、将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.二氧化硅中含有4mol硅氧键,据此计算出二氧化硅及氧原子的物质的量;
B.重水的摩尔质量为20g/mol,1.8g重水的物质的量为0.09mol,含有质子和电子的物质的量都是0.9mol;
C.醋酸根离子在溶液中部分水解,导致醋酸根离子数目减少;
D.没有告诉在标况下,题中条件无法计算氯气的物质的量.
B.重水的摩尔质量为20g/mol,1.8g重水的物质的量为0.09mol,含有质子和电子的物质的量都是0.9mol;
C.醋酸根离子在溶液中部分水解,导致醋酸根离子数目减少;
D.没有告诉在标况下,题中条件无法计算氯气的物质的量.
解答:
解:A.含有4mol硅氧键,需要1mol二氧化硅,1mol二氧化硅中含有2mol氧原子,含有的氧原子数为2NA,故A正确;
B.1.8g重水的物质的量为0.09mol,0.09mol重水中含有的质子和中子的物质的量都是0.9mol,含有的质子数和电子数均为0.9NA,故B错误;
C.1 L 1mol?L-1的CH3COONa溶液中含有溶质醋酸钠1mol,由于醋酸根离子部分水解,溶液中醋酸根离子的物质的量小于1mol,含有CH3COO-的数目小于NA,故C错误;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算11.2L氯气的物质的量,故D错误;
故选A.
B.1.8g重水的物质的量为0.09mol,0.09mol重水中含有的质子和中子的物质的量都是0.9mol,含有的质子数和电子数均为0.9NA,故B错误;
C.1 L 1mol?L-1的CH3COONa溶液中含有溶质醋酸钠1mol,由于醋酸根离子部分水解,溶液中醋酸根离子的物质的量小于1mol,含有CH3COO-的数目小于NA,故C错误;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算11.2L氯气的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项D为易错点,注意题中没有告诉在标况下.

练习册系列答案
相关题目
下列装置或操作能达到实验目的是( )
A、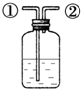 用排饱和食盐水法收集氯气,瓶内装饱和食盐水,氯气从①口进,②口出 |
B、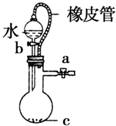 该装置中橡皮管的作用是能使水顺利流下 |
C、 除去苯中的己烷 |
D、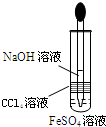 制备Fe(OH)2 |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 配制100mL 0.1mol?L-1的硫酸 |
B、 吸收氨气并防止倒吸 |
C、 制取少量乙烯气体 |
D、 验证溴乙烷发生消去反应 |
下列表示对应化学反应的离子方程式正确的是( )
| A、向铁粉中加入足量稀硝酸:2Fe+6H+═2Fe3++3H2↑ |
| B、向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-═AlO2-+2H2O |
| C、向NaIO3溶液中加入适量NaHSO3溶液:IO3-+3HSO3-═I-+3SO42-+3H+ |
| D、向NH4HCO3溶液中滴加过量NaOH溶液:NH4++HCO3-+2OH-═CO32-+NH3?H2O |
NA为阿伏加德罗常数,下列叙述错误的是( )
| A、0.1mol Na2O2与足量水完全反应时,转移电子数目为0.1NA |
| B、12g金刚石含有的共价键数为2NA |
| C、0.1mol的铜与足量的浓硫酸反应生成SO2的体积(标况)约为2.24L |
| D、标况下,22.4L CH3Cl和CH2Cl2的混合物所含氯原子数介于NA至2NA之间 |
下列变化可通过一步化学反应实现的是( )
| A、S→S03 |
| B、Al203→Al( OH)3 |
| C、Si02→H2SiO3 |
| D、Na2CO3→NaOH |