题目内容
6.25℃时,0.001mol/L的盐酸溶液的pH等于( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
分析 根据盐酸为一元强酸计算氢离子浓度,再根据pH=-lgc(H+)计算;
解答 解:盐酸为一元强酸完全电离,0.001mol/L的盐酸氢离子浓度c(H+)=0.001mol/L,pH=-lgc(H+)=-lg0.001=3,
故选B.
点评 本题考查了溶液pH的计算,题目难度不大,注意掌握溶液酸碱性与溶液pH的计算方法,明确酸溶液的pH的计算方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
16.不用其他试剂就可以鉴别的一组是( )
| A. | 碳酸氢钙溶液和氢氧化钠 | B. | 碳酸钠溶液和硫酸 | ||
| C. | 偏铝酸钠溶液和氢氧化钠 | D. | 硫酸氢钠溶液和氯化钡溶液 |
17.下列各组粒子不能互称为等电子体的是( )
| A. | CO和N2 | B. | N2H4和 C2H4 | C. | CO2和N2O | D. | O3和SO2 |
14.下列表示物质结构的化学用语或模型正确的是( )
| A. | 8个中子的碳原子的符号:14C | B. | N2的电子式:N:::N: | ||
| C. | Cl-离子的结构示意图: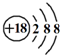 | D. | HF的电子式:H+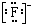 |
1.甘氨酸(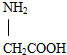 )和丙氨酸(
)和丙氨酸(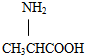 )缩合最多可形成( )种二肽.
)缩合最多可形成( )种二肽.
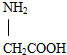 )和丙氨酸(
)和丙氨酸(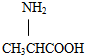 )缩合最多可形成( )种二肽.
)缩合最多可形成( )种二肽.| A. | 1 | B. | 2 | C. | 4 | D. | 3 |
11.下列化学用语正确的是( )
| A. | 乙醛的结构简式是:CH3CHO | |
| B. | 乙烯的球棍模型 | |
| C. | CCl4的电子式为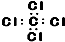 | |
| D. | 含中子数为10的氧元素的一种核素 10O |
18.下列说法正确的是( )
| A. | 往盛有500mL1mol/L的Na2CO3的溶液中滴加稀盐酸,可以观察到立即产生大量气泡 | |
| B. | 100mL 0.5mol/L氯酸钾溶液中含有氯离子的物质的量是0.05mol | |
| C. | 在开放的环境中往含有Fe2+,Al3+,Mg2+,Na+的溶液中滴加NaOH溶液,最终可以得到4种沉淀 | |
| D. | H+,NO3-,Fe2+,Mg2+不能共存 |
15.下列离子方程式书写正确的是( )
| A. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| B. | 铁溶于盐酸中:Fe+6H+═Fe3++3H2↑ | |
| C. | 氯化铝溶液和氨水反应 Al3++NH3•H2O═Al(OH)3↓+NH4+ | |
| D. | NaHCO3溶液与HCl溶液反应:H++HCO3-═CO2↑+H2O |
16.下列固体混合物中,能通过加热来分离的是( )
| A. | 氯酸钾和二氧化锰 | B. | 氯化铵和碘 | ||
| C. | 氯化铵和硫酸钠 | D. | 氯化钠和溴化钾 |