题目内容
下列物质的杂化方式不是sp3杂化的是( )
| A、CO2 |
| B、CH4 |
| C、NH3 |
| D、H2O |
考点:原子轨道杂化方式及杂化类型判断
专题:
分析:中心原子的杂化类型为sp3,说明该分子中心原子的价层电子对个数是4,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=
(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.
| 1 |
| 2 |
解答:
解:A.CO2中只含有双键,既有σ键又有π键,分子中C原子含有2个σ键电子对,没有孤电子对,价层电子对个数=2+0=2,杂化类型为sp,故A选;
B.CH4中只含有单键为σ键,分子中C原子含有4个σ键电子对,没有孤电子对,C原子杂化轨道数=δ键数+孤对电子对数=4+0=4,所以采取sp3杂化,故B不选;
C.氨气分子中氮原子价层电子对个数=3+
(5-3×1)=4,所以N原子采用sp3杂化,故C不选;
D.水中O原子杂化轨道数=σ键数+孤对电子对数=2+2=4,所以采取sp3杂化,故D不选;
故选A.
B.CH4中只含有单键为σ键,分子中C原子含有4个σ键电子对,没有孤电子对,C原子杂化轨道数=δ键数+孤对电子对数=4+0=4,所以采取sp3杂化,故B不选;
C.氨气分子中氮原子价层电子对个数=3+
| 1 |
| 2 |
D.水中O原子杂化轨道数=σ键数+孤对电子对数=2+2=4,所以采取sp3杂化,故D不选;
故选A.
点评:本题考查了原子杂化方式的判断,根据价层电子对互斥理论来分析解答即可,明确孤电子对个数=
(a-xb)中各个字母的含义,题目难度中等.
| 1 |
| 2 |

练习册系列答案
相关题目
有4种有机物:① ,②
,② ,③
,③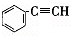 ,④CH3-CH=CH-CN,其中可用于合成
,④CH3-CH=CH-CN,其中可用于合成 结构简式为的高分子材料的正确组合为( )
结构简式为的高分子材料的正确组合为( )
 ,②
,② ,③
,③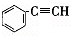 ,④CH3-CH=CH-CN,其中可用于合成
,④CH3-CH=CH-CN,其中可用于合成 结构简式为的高分子材料的正确组合为( )
结构简式为的高分子材料的正确组合为( )| A、①③④ | B、①②③ |
| C、①②④ | D、②③④ |
下列物质中,可用来制造铅笔的是( )
| A、石墨 | B、金刚石 | C、铁 | D、铅 |
已知:Ka1(H2CO3)>Ka(C6H5OH)>Ka2(H2CO3)下列反应不能发生的是(Ka1、Ka2各指一级、二级电离常数)
( )
( )
| A、H2CO3+CO32-→2HCO3- | ||
B、 +H2CO3→ +H2CO3→ +HCO +HCO
| ||
C、 +HCO3-→ +HCO3-→ +CO32- +CO32- | ||
D、 +CO32-→ +CO32-→ +HCO3- +HCO3- |
下列物质属于等电子体一组的是( )
| A、CH4和NH4+ |
| B、B3H6N3和C6H6 |
| C、CO2、NO2 |
| D、H2O和CH4 |
含ngHNO3的稀硝酸溶液恰好与mg铁粉完全反应,若HNO3只被还原为NO,则n:m可能是:①5:1②9:2③3:1④2:1⑤4:1( )
| A、②③⑤ | B、①③④ |
| C、②③ | D、①③⑤ |
雪是冬之精灵,雪
水
冰的转化中( )
| △H1 |
| △H2 |
| A、△H1>0,△H2>0 |
| B、△H1>0,△H2<0 |
| C、△H1<0,△H2<0 |
| D、△H1<0,△H2>0 |
居室装修用石材的放射性常用
Ra作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖.下列叙述中正确的是( )
226 88 |
| A、RaCl2的熔点比CaCl2高 | ||
| B、Ra元素位于元素周期表中第六周期ⅡA族 | ||
C、一个
| ||
| D、Ra(OH)2是一种两性氢氧化物 |