题目内容
实验题:实验室制取乙炔气体.
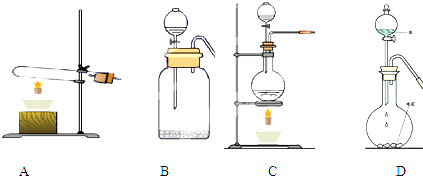
(1)可以作为乙炔发生装置的实验装置图有 ,与制 、 装置相同
(2)制取乙炔的化学反应方程式: 乙炔气体通入高锰酸钾溶液中观察到的现象是 ,乙炔发生了 反应.
(3)乙炔通入溴的四氯化碳溶液中,现象是 ,乙炔与溴反应方程式: ,反应类型: .
(4)除去乙炔含有的气体杂质,将气体通入 溶液.为了安全,点燃乙炔前应 ,乙炔燃烧的现象是 ,收集乙炔的方法是 .
(1)可以作为乙炔发生装置的实验装置图有

(2)制取乙炔的化学反应方程式:
(3)乙炔通入溴的四氯化碳溶液中,现象是
(4)除去乙炔含有的气体杂质,将气体通入
考点:常见气体制备原理及装置选择,乙炔的性质实验
专题:实验题
分析:(1)实验室通过电石与水的反应制取乙炔,是固+液
气装置,制取氢气、二氧化碳也采用此类装置;
(2)实验室通过电石与水的反应制取乙炔,以此写出化学方程式,乙炔能使酸性高锰酸钾溶液褪色,发生氧化反应;
(3)乙炔能使溴的四氯化碳溶液褪色发生加成反应;
(4)电石主要成分是CaC2,还有杂质CaS Ca3P2等,这些杂质CaS Ca3P2也能和水反应,生成H2S,PH3等杂质,可以用硫酸铜溶液除去;可燃性气体在点燃前必须检验其纯度,以免发生爆炸.因乙炔中含碳的质量分数较大,在燃烧时火焰明亮并伴有浓烈的黑烟,乙炔不溶于水,可采用排水法收集.
| 不加热 |
(2)实验室通过电石与水的反应制取乙炔,以此写出化学方程式,乙炔能使酸性高锰酸钾溶液褪色,发生氧化反应;
(3)乙炔能使溴的四氯化碳溶液褪色发生加成反应;
(4)电石主要成分是CaC2,还有杂质CaS Ca3P2等,这些杂质CaS Ca3P2也能和水反应,生成H2S,PH3等杂质,可以用硫酸铜溶液除去;可燃性气体在点燃前必须检验其纯度,以免发生爆炸.因乙炔中含碳的质量分数较大,在燃烧时火焰明亮并伴有浓烈的黑烟,乙炔不溶于水,可采用排水法收集.
解答:
解:(1)实验室通过电石与水的反应制取乙炔,是固+液
气装置,因此可选择装置BD,与制取氢气、二氧化碳装置相同,
故答案为:BD;H2;CO2 ;
(2)实验室通过电石与水的反应制取乙炔,化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑,乙炔含有不饱和键,能使酸性高锰酸钾溶液褪色,发生氧化反应,
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;褪色;氧化;
(3)乙炔能够和溴水发生加成反应,化学方程式为C2H2+2Br2=CHBr2CHBr2,因此现象为溴的四氯化碳溶液褪色,
故答案为:溴的四氯化碳溶液褪色;C2H2+2Br2→CHBr2CHBr2;加成;
(4)电石主要成分是CaC2,还有杂质CaS Ca3P2等,这些杂质CaS Ca3P2也能和水反应,生成H2S,PH3等杂质,可以用硫酸铜溶液除去,乙炔是可燃性气体,可燃性气体在点燃前必须检验其纯度,以免发生爆炸.因乙炔中含碳的质量分数较大,在燃烧时火焰明亮并伴有浓烈的黑烟,乙炔不溶于水,可采用排水法收集,
故答案为:硫酸铜溶液;验纯;火焰明亮,并伴有黑烟;排水法.
| 不加热 |
故答案为:BD;H2;CO2 ;
(2)实验室通过电石与水的反应制取乙炔,化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑,乙炔含有不饱和键,能使酸性高锰酸钾溶液褪色,发生氧化反应,
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;褪色;氧化;
(3)乙炔能够和溴水发生加成反应,化学方程式为C2H2+2Br2=CHBr2CHBr2,因此现象为溴的四氯化碳溶液褪色,
故答案为:溴的四氯化碳溶液褪色;C2H2+2Br2→CHBr2CHBr2;加成;
(4)电石主要成分是CaC2,还有杂质CaS Ca3P2等,这些杂质CaS Ca3P2也能和水反应,生成H2S,PH3等杂质,可以用硫酸铜溶液除去,乙炔是可燃性气体,可燃性气体在点燃前必须检验其纯度,以免发生爆炸.因乙炔中含碳的质量分数较大,在燃烧时火焰明亮并伴有浓烈的黑烟,乙炔不溶于水,可采用排水法收集,
故答案为:硫酸铜溶液;验纯;火焰明亮,并伴有黑烟;排水法.
点评:本题考查了乙炔的实验室制法和性质,难度不大,明确乙炔的结构和性质是解题的关键,注意相关知识的积累.

练习册系列答案
相关题目
如图为反应N2+3H2?2NH3的速率V(N2)变化的图象,则横坐标不可能是( )


| A、反应时间 |
| B、温度 |
| C、压强 |
| D、N2的浓度 |
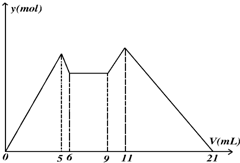 如图所示,是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,6ml后继续滴加A若干,之后改滴试剂B,所得 沉淀ymol 与试剂体积V(ml)间的关系.以下结论错误的是( )
如图所示,是向MgCl2、AlCl3混合溶液中,开始滴加6ml试剂A,6ml后继续滴加A若干,之后改滴试剂B,所得 沉淀ymol 与试剂体积V(ml)间的关系.以下结论错误的是( )| A、从6到9,相应离子反应式H++OH-=H2O |
| B、原混合液中,c(Al3+):c(Mg2+):c(Cl-)=1:1:5 |
| C、A可能是NaOH,B可能是盐酸,且c(NaOH):c(HCl)=1:2 |
| D、若A,B均为一元强酸或者一元强碱,则V(A):V(B)=7:13 |
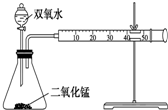 某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表: 实验室里需用480mL 0.1mol?L-1的硫酸铜溶液.试回答该溶液配制过程中的下列问题:
实验室里需用480mL 0.1mol?L-1的硫酸铜溶液.试回答该溶液配制过程中的下列问题: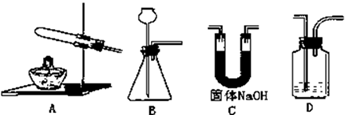 ①实验室制氧气时,应选用的发生装置是
①实验室制氧气时,应选用的发生装置是