题目内容
为除去羰基硫,工业上常采用催化加氢转化法,把羰基硫转化为H2S再除去:COS+H2═CO+H2S
(1)已知升高温度,会降低羰基硫的转化率.则升高温度,平衡常数K ,反应速率 (均选填“增大”、“减小”、“不变”).
(2)若反应在恒容绝热密闭容器中进行,能说明该反应已达到平衡状态的是 .
a.容器内气体密度保持不变 b.容器内温度保持不变
c.c(H2)=c(H2S) d.υ(H2)正=υ(H2S)正
(3)已知该反应的平衡常数很大,说明 .
(1)已知升高温度,会降低羰基硫的转化率.则升高温度,平衡常数K
(2)若反应在恒容绝热密闭容器中进行,能说明该反应已达到平衡状态的是
a.容器内气体密度保持不变 b.容器内温度保持不变
c.c(H2)=c(H2S) d.υ(H2)正=υ(H2S)正
(3)已知该反应的平衡常数很大,说明
考点:化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)升高温度,会降低羰基硫的转化率,说明平衡逆向进行,逆向是吸热反应;升温增大反应速率,正逆反应速率增大;
(2)反应在恒容绝热密闭容器中进行,反应达到平衡状态正逆反应速率相同,各成分含量不变;
(3)平衡常数是衡量反应进行程度的物理量,平衡常数越大反应进行越彻底.
(2)反应在恒容绝热密闭容器中进行,反应达到平衡状态正逆反应速率相同,各成分含量不变;
(3)平衡常数是衡量反应进行程度的物理量,平衡常数越大反应进行越彻底.
解答:
解:(1)升高温度,会降低羰基硫的转化率,说明平衡逆向进行,逆向是吸热反应,平衡常数减小;升温增大反应速率,正逆反应速率增大;
故答案为:减小;增大;
(2)反应在恒容绝热密闭容器中进行,反应达到平衡状态正逆反应速率相同,各成分含量不变;
a.容器内气体密度保持不变,不能说明反应达到平衡状态,故a不符合;
b.恒容绝热密闭容器中进行,容器内温度保持不变,说明反应达到平衡状态,故b符合;
c.浓度相同和起始量变化量有关,c(H2)=c(H2S) 不能说明反应达到平衡状态,故c不符合;
d.反应速率之比等于化学方程式系数之比,表示的是正反应速率之比,υ(H2)正=υ(H2S)正 ,不能说明 反应达到平衡状态,故d不符合;
故答案为:b;
(3)平衡常数是衡量反应进行程度的物理量,平衡常数越大反应进行越彻底;
故答案为:反应进行程度越大.
故答案为:减小;增大;
(2)反应在恒容绝热密闭容器中进行,反应达到平衡状态正逆反应速率相同,各成分含量不变;
a.容器内气体密度保持不变,不能说明反应达到平衡状态,故a不符合;
b.恒容绝热密闭容器中进行,容器内温度保持不变,说明反应达到平衡状态,故b符合;
c.浓度相同和起始量变化量有关,c(H2)=c(H2S) 不能说明反应达到平衡状态,故c不符合;
d.反应速率之比等于化学方程式系数之比,表示的是正反应速率之比,υ(H2)正=υ(H2S)正 ,不能说明 反应达到平衡状态,故d不符合;
故答案为:b;
(3)平衡常数是衡量反应进行程度的物理量,平衡常数越大反应进行越彻底;
故答案为:反应进行程度越大.
点评:本题考查了化学平衡、平衡常数的影响因素分析,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
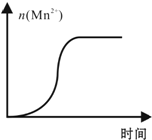 KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去.某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响.该实验条件作如下限定:
KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去.某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响.该实验条件作如下限定:
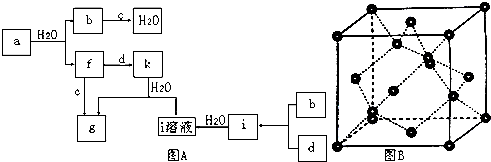
 某课外活动小组用如图装置进行实验,试回答下列问题.
某课外活动小组用如图装置进行实验,试回答下列问题.