题目内容
11.下列离子方程式书写正确的是( )| A. | 碳酸钙溶于盐酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 钠投入水中:Na+H2O═Na++2OH-+H2↑ | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氢氧化钡溶液滴入稀硫酸中:Ba2++SO42-═BaSO4↓ |
分析 A.反应生成氯化钙和水、二氧化碳;
B.电子、电荷不守恒;
C.反应生成硫酸亚铁和氢气;
D.漏写生成水的离子反应.
解答 解:A.碳酸钙溶于盐酸的离子反应为CaCO3+2H+═Ca2++H2O+CO2↑,故A正确;
B.钠投入水中的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故B错误;
C.铁粉加入稀硫酸中的离子反应为Fe+2H+═Fe2++H2↑,故C错误;
D.氢氧化钡溶液滴入稀硫酸中的离子反应为2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
1.100mL 1mol•L-1Al2(SO4)3溶液中,含Al3+离子的物质的量( )
| A. | 0.1mol | B. | 0.2mol | C. | 0.3mol | D. | 0.4mol |
2.既能通过金属单质与足量Cl2反应得到,也能通过金属单质与酸反应得到的是( )
| A. | FeCl2 | B. | NaCl | C. | FeCl3 | D. | CuCl2 |
16.下列配制溶液的操作中,不会影响所配溶液浓度大小的是…( )
| A. | 托盘两边各垫一张质量相等的纸片称取固体NaOH | |
| B. | 容量瓶内水分未干便注入了液体 | |
| C. | 洗涤刚才盛过溶质的烧杯的洗涤液没有转入容量瓶 | |
| D. | 定容后使溶液混匀,静止,发现凹液面低于刻度线,立即滴加蒸馏水至刻度线 |
3.下列反应中,在高温下不能自发进行的是( )
| A. | 2CO(g)═2C(s)+O2(g) | B. | NH4Cl(s)=NH3(g)+HCl(g) | ||
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g) | D. | MgCO3(s)═MgO(s)+CO2(g) |
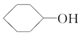 ④
④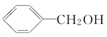 ⑤
⑤