题目内容
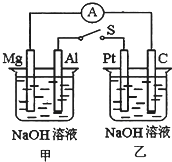 如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )| A、电流表指针不发生偏转 |
| B、Al、Pt两极有H2产生 |
| C、甲池pH减小,乙池pH不变 |
| D、Mg、C两极生成的气体可以恰好完全反应 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:关闭开关S甲装置形成原电池反应,铝做负极失电子发生氧化反应,镁做正极,电极上得到电子发生还原反应,乙池为电解池,Pt做电解池阴极,C做电解池的阳极;
A.电流计有电流通过;
B.铝电极是原电池负极溶解无气体生成,Pt电极上氢离子得到电子生成氢气;
C.甲装置是原电池消耗氢氧根离子,溶液PH减小;乙池是电解池,电极水溶液浓度增大,氢氧化钠溶液PH增大;
D.镁电极生成的氢气,C电极生成的是氧气.
A.电流计有电流通过;
B.铝电极是原电池负极溶解无气体生成,Pt电极上氢离子得到电子生成氢气;
C.甲装置是原电池消耗氢氧根离子,溶液PH减小;乙池是电解池,电极水溶液浓度增大,氢氧化钠溶液PH增大;
D.镁电极生成的氢气,C电极生成的是氧气.
解答:
解:关闭开关S甲装置形成原电池反应,铝做负极失电子发生氧化反应,镁做正极,电极上得到电子发生还原反应,乙池为电解池,Pt做电解池阴极,C做电解池的阳极;
A.甲装置形成的原电池,反应过程中有电子转移产生电流,电流计有电流通过,故A错误;
B.铝电极是原电池负极溶解无气体生成,Pt电极上氢离子得到电子生成氢气,故B错误;
C.甲装置是原电池消耗氢氧根离子,溶液pH减小;乙池是电解池,电极水溶液浓度增大,氢氧化钠溶液pH增大,故C错误;
D.镁电极生成的氢气,C电极生成的是氧气,依据电子守恒可知生成2mol氢气同时生成1mol氧气,氢气和氧气恰好反应生成水,故D正确;
故选D.
A.甲装置形成的原电池,反应过程中有电子转移产生电流,电流计有电流通过,故A错误;
B.铝电极是原电池负极溶解无气体生成,Pt电极上氢离子得到电子生成氢气,故B错误;
C.甲装置是原电池消耗氢氧根离子,溶液pH减小;乙池是电解池,电极水溶液浓度增大,氢氧化钠溶液pH增大,故C错误;
D.镁电极生成的氢气,C电极生成的是氧气,依据电子守恒可知生成2mol氢气同时生成1mol氧气,氢气和氧气恰好反应生成水,故D正确;
故选D.
点评:本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力的考查,正确判断原电池和电解池及其正负极和阴阳极是解本题关键,明确离子的放电顺序,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
一定温度下,反应X(g)+3Y(g)?2Z(g)达化学平衡状态的标志是( )
| A、Z的生成速率与Z的分解速率相等 |
| B、单位时间生成amolX,同时生成3amolY |
| C、X、Y、Z的浓度相等 |
| D、X、Y、Z的分子数比为1:3:2 |
一种新型的燃料电池,它以多孔的镍板为电极插入KOH溶液中,然后分别向两极上通乙烷和氧气,其电极反应式为:C2H6+18OH--14e=2CO32-+12H2O,7H2O+(
)O2+14e=14OH-下列有关此电池的推断正确的是( )
| 7 |
| 2 |
| A、电解质溶液中CO32-向正极移动 |
| B、放电一段时间后,KOH的物质的量浓度不变 |
| C、通乙烷的电极为负极 |
| D、参加反应的O2和C2H6的物质的量之比为7:1 |
实验室里熔化氢氧化钠时,应选用的坩埚是( )
| A、氧化铝坩埚 | B、石英坩埚 |
| C、铁坩埚 | D、瓷坩埚 |
下列说法正确的是( )
| A、光纤有广泛的用途.制造光纤的主要材料是单质硅 |
| B、氢氧化钠、碳酸氢钠、氢氧化铝都可用作抗酸药 |
| C、甲醛的水溶液具有杀菌、防腐的作用,可用于海产品保鲜 |
| D、水垢中含有的硫酸钙可用饱和碳酸钠溶液处理,使之转化为碳酸钙 |
下列叙述中,正确的是( )
| A、自然界中存在大量单质硅 | ||||
| B、硅元素是形成地壳的主要元素,在地壳中的含量占第一位 | ||||
C、纯硅可以通过下列反应制得:SiO2+2C
| ||||
| D、单晶硅是良好的半导体材料 |
能正确表示下列反应的离子方程式是( )
| A、醋酸钠的水解反应 CH3COO-+H3O+=CH3COOH+H2O |
| B、碳酸氢钙与过量的NaOH溶液反应 Ca2++2HCO3-+2OH -=CaCO3↓+2H2O+CO32- |
| C、苯酚钠溶液与二氧化碳反应 C6H5O-+CO2+H2O=C6H5OH+CO32- |
| D、稀硝酸与过量的铁屑反应 3Fe+8H++2 NO3-=3Fe 3++2NO↑+4H2O |
