题目内容
实验室检验海带中含有碘元素的主要步骤如下,回答相关问题.
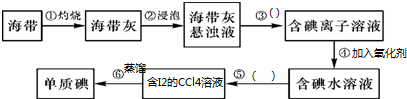
(1)④中可以选择的氧化剂有:氯水,酸化的双氧水,酸化的高锰酸钾,从绿色化学的角度来考虑,最理想的氧化剂为 ,反应的离子方程式为 .
(2)写出图中③、⑤的操作名称 , .

(1)④中可以选择的氧化剂有:氯水,酸化的双氧水,酸化的高锰酸钾,从绿色化学的角度来考虑,最理想的氧化剂为
(2)写出图中③、⑤的操作名称
考点:海水资源及其综合利用
专题:实验设计题
分析:海带灼烧得到海带灰硫浸泡得到海带灰悬浊液,过滤得到含碘离子的溶液,加入氧化剂氧化碘离子为碘单质,加入四氯化碳萃取分液得到含碘单质的四氯化碳溶液,蒸馏得到单质碘.
解答:
解:海带灼烧得到海带灰硫浸泡得到海带灰悬浊液,过滤得到含碘离子的溶液,加入氧化剂氧化碘离子为碘单质,加入四氯化碳萃取分液得到含碘单质的四氯化碳溶液,蒸馏得到单质碘;
(1)④中可以选择的氧化剂有:氯水,酸化的双氧水,酸化的高锰酸钾,从绿色化学的角度来考虑,最理想的氧化剂是酸化的双氧水,过氧化氢在酸溶液中氧化碘离子为碘单质,反应的离子方程式为:H2O2+2H++2I-=I2+2H2O;
故答案为:酸化的双氧水;H2O2+2H++2I-=I2+2H2O;
(2)依据流程分析可知步骤③是过滤,⑤是萃取分液,故答案为:过滤;萃取分液.
(1)④中可以选择的氧化剂有:氯水,酸化的双氧水,酸化的高锰酸钾,从绿色化学的角度来考虑,最理想的氧化剂是酸化的双氧水,过氧化氢在酸溶液中氧化碘离子为碘单质,反应的离子方程式为:H2O2+2H++2I-=I2+2H2O;
故答案为:酸化的双氧水;H2O2+2H++2I-=I2+2H2O;
(2)依据流程分析可知步骤③是过滤,⑤是萃取分液,故答案为:过滤;萃取分液.
点评:本题考查了海水提取碘的流程分析判断,注意过程中试剂选择和实验基本操作,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
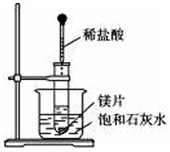
如图关于仪器的识别错误的是( )
A、 分液漏斗 |
B、 蒸发皿 |
C、 坩埚钳 |
D、 滴瓶 |
下列说法中正确的是( )
| A、101kPa时,1mol纯物质燃烧生成氧化物时所放出的热量,就是燃烧热 |
| B、生成物成键时所释放的总能量大于断键时所吸收的总能量,反应为吸热反应 |
| C、1mol稀酸与1mol稀碱发生中和反应生成水时所放出的热量,就是中和热 |
| D、生成物的总能量大于反应物的总能量时,反应吸热,△H>0 |
在下列各组离子中,能大量共存的是( )
| A、Al3+、NH4+、AlO2-、Cl- |
| B、Cu2+、Fe2+、ClO-、SO42- |
| C、Na+、Ca2+、HCO3-、OH- |
| D、Cu2+、Fe3+、Cl-、NO3- |
 Ⅰ、在下列化合物中:H2O、Na2O、NaCl、KOH、CO2、NH4Cl、Na2O2、H 2O2、CH4、N2,请填空:
Ⅰ、在下列化合物中:H2O、Na2O、NaCl、KOH、CO2、NH4Cl、Na2O2、H 2O2、CH4、N2,请填空: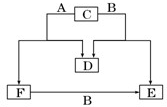 A、B、C、D、E、F六种物质中A、B、D常温下为气体,除D为单质外其余5种均为常见的化合物,E的水溶液呈中性,且能与硝酸银生成难溶于硝酸的白色沉淀,F的水溶液呈碱性,且E和F都为重要的化工原料,其焰色反应为黄色,它们的转化关系如图所示.请回答下列问题:
A、B、C、D、E、F六种物质中A、B、D常温下为气体,除D为单质外其余5种均为常见的化合物,E的水溶液呈中性,且能与硝酸银生成难溶于硝酸的白色沉淀,F的水溶液呈碱性,且E和F都为重要的化工原料,其焰色反应为黄色,它们的转化关系如图所示.请回答下列问题: