题目内容
15.+6价铬的毒性很强,制取红矾钠后的废水中含有的Cr2O72-,可以用绿矾除去.测得反应后的溶液中含Cr3+、Fe2+、Fe3+、H+等阳离子.写出该反应的离子方程式:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.分析 Cr2O72-有强氧化性,亚铁离子有还原性,亚铁离子能被氧化生成铁离子,同时Cr2O72-被还原生成铬离子,结合电子、原子守恒守恒配平方程式,以此来解答.
解答 解:Cr元素由Cr2O72-中+6价降低为Cr3+中+3价,共降低6价,Fe元素化合价由Fe2+中+2价升高为Fe3+中+3价,共升高1价,化合价最小公倍数为6,故Cr2O72-系数为1,Fe2+的系数为6,由原子守恒可知,Cr3+的系数为2,Fe3+的系数为6,根据电荷守恒可知,H+为反应物,系数为14,由H元素守恒,H2O为生成物,系数为7,则离子反应方程式为Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O,
故答案为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应中遵循电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
5.既有离子键又有共价键的化合物是( )
| A. | Na2O | B. | H2O2 | C. | CH4 | D. | NaOH |
6.下列有关化学键的叙述,正确的是( )
| A. | 离子化合物中一定含有离子键 | |
| B. | 常温呈气态的单质分子中均存在共价键 | |
| C. | 含有极性键的分子一定是极性分子 | |
| D. | 含有共价键的化合物一定是共价化合物 |
3.面粉是制作面包的主要原料,判断面粉品质优劣的测定项目通常有:淀粉含量.灰分含量及面粉酸度等.面粉酸度的度数是指中和100克面粉中含有的酸所耗用质量分数为0.4%氢氧化钠溶液的毫升数.面粉酸度与面粉品质的关系如表.
面粉酸度与面粉品质的关系表
请回答:
(1)为检测某种面粉中是否含有淀粉,取一定质量的面粉放入烧杯中,加入适量的蒸馏水,搅拌,缓缓加热,溶解,取少量试液置于试管中,滴加碘液,若溶液变蓝色,就说明该面粉中含有淀粉.
(2)称取5克某种面粉放入锥形瓶,加入适量蒸馏水搅匀,为减小实验误差,现用质量分数为0.004%氢氧化钠溶液来进行测定,恰好完全反应时共消耗22毫升氢氧化钠溶液.计算该面粉的酸度4.4°;,并判断其品质(忽略两种氢氧化钠溶液密度的差异)陈年面粉.
面粉酸度与面粉品质的关系表
| 面粉酸度 | <2° | 2°-4.5° | >4.5° |
| 面粉品质 | 新鲜面粉 | 陈年面粉 | 霉变面粉 |
(1)为检测某种面粉中是否含有淀粉,取一定质量的面粉放入烧杯中,加入适量的蒸馏水,搅拌,缓缓加热,溶解,取少量试液置于试管中,滴加碘液,若溶液变蓝色,就说明该面粉中含有淀粉.
(2)称取5克某种面粉放入锥形瓶,加入适量蒸馏水搅匀,为减小实验误差,现用质量分数为0.004%氢氧化钠溶液来进行测定,恰好完全反应时共消耗22毫升氢氧化钠溶液.计算该面粉的酸度4.4°;,并判断其品质(忽略两种氢氧化钠溶液密度的差异)陈年面粉.
10.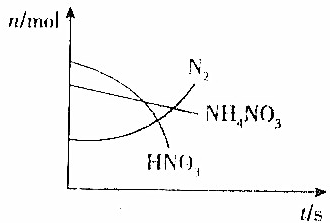 某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )
某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )
 某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )
某容器中发生一个化学反应,反应过程中存在Zn、H2O、HNO3、N2、NH4NO3和Zn(NO3)2六种物质,在反应过程中测得HNO3、NH4NO3和N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )| A. | N2是还原产物,Zn(NO3)2是氧化产物 | |
| B. | NH4NO3是氧化剂,Zn是还原剂 | |
| C. | 反应生成1molN2时共有5mol电子转移 | |
| D. | HNO3在反应中没有表现出酸性 |




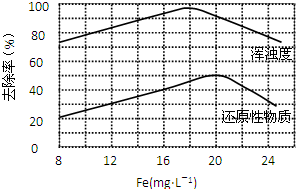 FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小.请回答下列问题:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小.请回答下列问题: