题目内容
高纯硅生产流程如图:

(1)由SiO2制粗硅的化学方程式是 ,该反应不能说明碳的非金属性强于硅,原因是 ,请写出一个能说明碳的非金属性强于硅的化学方程式 .
(2)900℃以上,H2与SiHCl3发生反应:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)△H>0.将一定量的反应物通入固定容积的密闭容器中进行反应.下列说法正确的是 (填字母).
a.在恒温条件下,若容器内压强不变,则该反应一定达到化学平衡状态
b.增大SiHCl3的用量,可提高SiHCl3的平衡转化率
c.升高温度可加快反应速率,且提高硅的产率
(3)该流程中可以循环使用的物质是 .

(1)由SiO2制粗硅的化学方程式是
(2)900℃以上,H2与SiHCl3发生反应:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)△H>0.将一定量的反应物通入固定容积的密闭容器中进行反应.下列说法正确的是
a.在恒温条件下,若容器内压强不变,则该反应一定达到化学平衡状态
b.增大SiHCl3的用量,可提高SiHCl3的平衡转化率
c.升高温度可加快反应速率,且提高硅的产率
(3)该流程中可以循环使用的物质是
考点:硅和二氧化硅,化学平衡的影响因素
专题:化学平衡专题,元素及其化合物
分析:(1)碳与二氧化硅反应生成硅单质和一氧化碳,只能说明碳的还原性比硅强,强酸反应制取弱酸;
(2)a.反应前后有气体物质的量的变化;
b.增大SiHCl3的用量,可提高H2的平衡转化率;
c.正反应是吸热反应;
(3)根据化学根据反应物中和生成物中都有的物质考虑.
(2)a.反应前后有气体物质的量的变化;
b.增大SiHCl3的用量,可提高H2的平衡转化率;
c.正反应是吸热反应;
(3)根据化学根据反应物中和生成物中都有的物质考虑.
解答:
解:(1)碳与二氧化硅反应生成硅单质和一氧化碳:SiO2+2C
Si+2CO,只能说明碳的还原性比硅强,非金属性是指非金属元素的单质在化学反应中得到电子的能力,不能说明碳的非金属性比硅强;非金属性较强的元素,对应的最高价氧化物的水化物的酸性较强,如碳的非金属性比硅强,则碳酸的酸性比硅酸强,可发生:Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3,
故答案为:SiO2+2C
Si+2CO;非金属性是指非金属元素的单质在化学反应中得到电子的能力,而碳与二氧化硅反应所表现出来的是碳失去电子的能力(或还原性),因此不能说明碳的非金属性比硅强;Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3;
(2)a.反应前后有气体物质的量的变化,若容器内压强不变,则该反应一定达到化学平衡状态,故a正确;
b.增大SiHCl3的用量,SiHCl3的平衡转化率降低,故b错误;
c.正反应是吸热反应,升温向正反应方向移动,且提高硅的产率,故c正确;
故答案为:ac;
(3)由图示可知反应物有粗硅、HCl、H2;反应过程中生成物有:SiHCl3、H2、SiCl4、HCl,所以在反应物中和生成物中都有的物质是HCl、H2,所以流程中可循环使用的物质是HCl、H2;
故答案为:HCl、H2.
| ||
故答案为:SiO2+2C
| ||
(2)a.反应前后有气体物质的量的变化,若容器内压强不变,则该反应一定达到化学平衡状态,故a正确;
b.增大SiHCl3的用量,SiHCl3的平衡转化率降低,故b错误;
c.正反应是吸热反应,升温向正反应方向移动,且提高硅的产率,故c正确;
故答案为:ac;
(3)由图示可知反应物有粗硅、HCl、H2;反应过程中生成物有:SiHCl3、H2、SiCl4、HCl,所以在反应物中和生成物中都有的物质是HCl、H2,所以流程中可循环使用的物质是HCl、H2;
故答案为:HCl、H2.
点评:本题涉及关硅和二氧化硅性质的综合题,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度较大,注意相关知识的积累.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
圆底烧瓶中加入的反应物是溴化钠、乙醇和1:1的硫酸.配制体积比1:1的硫酸所用的定量仪器为 ( )(选填编号).
| A、天平 | B、量筒 |
| C、容量瓶 | D、滴定管. |
下列分子中,各原子均处于同一平面上的是( )
| A、NH3 |
| B、CCl4 |
| C、SO32- |
| D、CH2O |
在乙酸乙酯、乙醇、乙酸水溶液共存的化学平衡体系中加入含重氢的水,经过足够长的时间后,可以发现,除水外体系中含重氢的化合物是( )
| A、只有乙醇 |
| B、乙酸、乙醇 |
| C、只有乙酸乙酯 |
| D、乙酸乙酯、乙醇、乙酸 |
研究出元素周期律并列出第一张元素周期表的伟大科学家是( )
| A、门捷列夫 | B、哈伯 |
| C、舍勒 | D、侯德榜 |

 四种元素A、B、C、D位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为50;A元素原子的核外只有一个电子;B元素原子的L层p轨道中有2个电子;C元素原子与B元素原子的价层电子数相同;D原子的最外层电子数为1,其d轨道中的电子数与K层电子数之比为5:1.
四种元素A、B、C、D位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为50;A元素原子的核外只有一个电子;B元素原子的L层p轨道中有2个电子;C元素原子与B元素原子的价层电子数相同;D原子的最外层电子数为1,其d轨道中的电子数与K层电子数之比为5:1.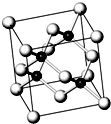 砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措.已知砷化镓的晶胞结构如图.试回答下列问题:
砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措.已知砷化镓的晶胞结构如图.试回答下列问题: