题目内容
除去食盐中混有的少量碘化钠杂质应采用的方法是( )
| A、加入AgNO3溶液后加热蒸干 |
| B、加入适量盐酸后加热蒸干 |
| C、加水溶解后通入适量氯气再加热蒸干 |
| D、加水溶解后滴入适量溴水再加热蒸干 |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:食盐中混有的少量碘化钠杂质,可溶解后通入氯气,然后蒸干可得到NaCl,以此来解答.
解答:
解:A.NaCl、NaI均与硝酸银反应生成沉淀,不能除杂,故A错误;
B.NaI与盐酸不反应,不能除杂,故B错误;
C.加水溶解后通入适量氯气,与NaI反应生成NaCl,再加热蒸干即可,故C正确;
D.溴水与NaI反应生成NaBr,引入新杂质,故D错误;
故选C.
B.NaI与盐酸不反应,不能除杂,故B错误;
C.加水溶解后通入适量氯气,与NaI反应生成NaCl,再加热蒸干即可,故C正确;
D.溴水与NaI反应生成NaBr,引入新杂质,故D错误;
故选C.
点评:本题考查混合物的分离提纯,为高频考点,把握物质的性质及性质差异为解答的关键,侧重混合物除杂的考查,注意发生的反应及除杂的原则,题目难度不大.

练习册系列答案
相关题目
聚四氟乙烯(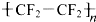 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
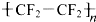 )是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )
)是不粘锅涂覆物质的主要成分.下列关于聚四氟乙烯的说法,不正确的是( )| A、属于高分子化合物 |
| B、单体是CF2=CF2 |
| C、可由加聚反应得到 |
| D、能使高锰酸钾酸性溶液褪色 |
在生活、生产中为增大反应速率而采取的措施合理的是( )
| A、塑料制品中添加抑制剂 |
| B、食物放在冰箱中 |
| C、燃煤发电时用煤粉代替煤块 |
| D、在糕点包装内放置小包除氧剂 |
下列比较正确的是( )
| A、化学键的键能由大到小:金刚石>碳化硅>硅>锗 |
| B、熔沸点由高到低:氯化钠>氧化铝>硅>二氧化碳 |
| C、硬度由大到小:C60>碳化硅>铁>氯化钠 |
| D、导电性能由强到弱:金>铜>石墨>二氧化碳 |
下列烷烃的分子式可以表示5种不同结构的是( )
| A、C4H10 |
| B、C5H12 |
| C、C6H14 |
| D、C7H16 |
某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,由此可以得出该有机物( )
| A、分子中C、H、O的个数比为1:2:3 |
| B、分子中C和H的个数比为1:2 |
| C、分子中肯定不一定含氧原子 |
| D、分子中肯定含有氧原子 |
下列化学式一定表示一种纯净物的是( )
| A、C2H6 |
| B、C2H4Br2 |
| C、C4H10 |
| D、C5H12 |
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量.在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ.下列关系式中正确的是( )
| A、Q1+Q2<2Q3 |
| B、Q1+Q2>2Q3 |
| C、Q1+Q2<Q3 |
| D、Q1+Q2>Q3 |