��Ŀ����
 �ݱ�����һ���������ɶ�����̼�������ϳ��Ҵ��ѳ�Ϊ��ʵ��
�ݱ�����һ���������ɶ�����̼�������ϳ��Ҵ��ѳ�Ϊ��ʵ����֪����CH3CH2OH��l��+3O2��g���T2CO2��g��+3H2O��l����H=-1366.8kJ/mol
��2H2��g��+O2��g���T2H2O��l����H=-571.6kJ/mol
��1��д����CO2��H2��Ӧ�ϳ�CH3CH2OH��l����H2O��l�����Ȼ�ѧ����ʽ
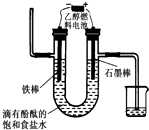
��2�������Ҵ�ȼ�ϵ���״��棬���ƹ㣬�Ի�����ȾС�����зdz������ķ�չǰ������ȼ�ϵ���У�ʹ�ò����缫��KOH��Һ���������Һ��ͨ���Ҵ�ȼ����һ��Ϊ
��3�����Ҵ�ȼ�ϵ�ص��400mL ����ʳ��ˮװ�ÿɼ�ʾ��ͼ����װ���з�����ⷴӦ�ķ���ʽΪ
���㣺��ѧ��Դ���͵��,�Ȼ�ѧ����ʽ
ר�⣺��ѧ��Ӧ�е������仯
��������1�����ݸ�˹���ɲ�����Ȼ�ѧ����ʽ�١���д����CO2 ��H2��Ӧ�ϳ�CH3CH2OH��l����H2O��l�����Ȼ�ѧ����ʽ��
��2��ԭ��صĸ�������������Ӧ���Ҵ�ȼ�ϵ���У��Ҵ������������Ը���Ϊ�Ҵ��ڼ�����Һ��ʧȥ��������̼������ӣ�
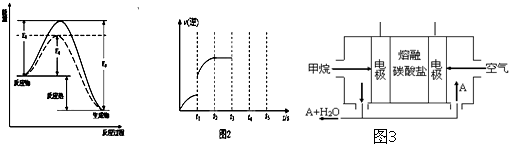
��3�����������缫���Դ�����ӷ�ʽ�жϵ��ص���������д����ⱥ��ʳ��ˮ�ķ���ʽ��Ȼ����ݵ�ⱥ��ʳ��ˮ�������ķ�Ӧ�жϷ�Ӧ������������������Ƶ����ʵ��������������Һ��pH��
��2��ԭ��صĸ�������������Ӧ���Ҵ�ȼ�ϵ���У��Ҵ������������Ը���Ϊ�Ҵ��ڼ�����Һ��ʧȥ��������̼������ӣ�
��3�����������缫���Դ�����ӷ�ʽ�жϵ��ص���������д����ⱥ��ʳ��ˮ�ķ���ʽ��Ȼ����ݵ�ⱥ��ʳ��ˮ�������ķ�Ӧ�жϷ�Ӧ������������������Ƶ����ʵ��������������Һ��pH��
���
�⣺��1����CH3CH2OH��l��+3O2��g��=2CO2��g��+3H2O��l����H=-1366.8kJ/mol��
��2H2��g��+O2��g��=2H2O��l����H=-571.6kJ/mol��
���ݸ�˹���ɣ��ڡ�3-�ٿɵã�2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=��-571.6kJ/mol����3-��-1366.8kJ/mol��=-348kJ/mol��
�ʴ�Ϊ��2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=-348kJ/mol��
��2�����Ҵ�ȼ�ϵ���У���������ȼ���Ҵ�����ʧ���ӵ�������Ӧ���ڼ��Ի����µĵ缫��ӦΪ��C2H6O+16OH--12e-=2CO32-+11H2O��
�ʴ�Ϊ������C2H6O+16OH--12e-=2CO32-+11H2O��
��3������ͼʾ��֪�����ĵ缫���ӵ�Դ�ĸ�����Ϊ���ص�����������������ԭ��Ӧ�����������Ҳ�����ԭ��ص�ֱ�ӣ����Ե��ص��Ҳ�Ϊ��������������������Ӧ�����������缫����ʳ��ˮ�ķ���ʽΪ��2NaCl+2H2O
Cl2��+H2��+2NaOH��
������ˮ����������ӷŵ磬ʹˮ�ĵ���ƽ�������ƶ�������������Ũ���������Դ��з�̪����Һ��죻
�������ɱ���µ�448mL���壬������Ϊ�����������448mL���������ʵ���Ϊ0.02mol�����ݷ�Ӧ����ʽ2NaCl+2H2O
Cl2��+H2��+2NaOH��֪������0.02mol����������0.04mol�������ƣ������Һ������������Ũ��Ϊ��c��OH-��=c��NaOH��=
=0.1mol/L����Һ��������Ũ��Ϊ��1��10-13mol/L����Һ��pH=13��
�ʴ�Ϊ��2NaCl+2H2O
Cl2��+H2��+2NaOH����Һ��죻13��
��2H2��g��+O2��g��=2H2O��l����H=-571.6kJ/mol��
���ݸ�˹���ɣ��ڡ�3-�ٿɵã�2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=��-571.6kJ/mol����3-��-1366.8kJ/mol��=-348kJ/mol��
�ʴ�Ϊ��2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=-348kJ/mol��
��2�����Ҵ�ȼ�ϵ���У���������ȼ���Ҵ�����ʧ���ӵ�������Ӧ���ڼ��Ի����µĵ缫��ӦΪ��C2H6O+16OH--12e-=2CO32-+11H2O��
�ʴ�Ϊ������C2H6O+16OH--12e-=2CO32-+11H2O��
��3������ͼʾ��֪�����ĵ缫���ӵ�Դ�ĸ�����Ϊ���ص�����������������ԭ��Ӧ�����������Ҳ�����ԭ��ص�ֱ�ӣ����Ե��ص��Ҳ�Ϊ��������������������Ӧ�����������缫����ʳ��ˮ�ķ���ʽΪ��2NaCl+2H2O
| ||
������ˮ����������ӷŵ磬ʹˮ�ĵ���ƽ�������ƶ�������������Ũ���������Դ��з�̪����Һ��죻
�������ɱ���µ�448mL���壬������Ϊ�����������448mL���������ʵ���Ϊ0.02mol�����ݷ�Ӧ����ʽ2NaCl+2H2O
| ||
| 0.04mol |
| 0.4L |
�ʴ�Ϊ��2NaCl+2H2O
| ||
���������⿼�����Ȼ�ѧ����ʽ����д��ԭ��ع���ԭ�����缫��Ӧʽ����д����Ŀ�Ѷ��еȣ�ע�������Ȼ�ѧ����ʽ����дԭ���ܹ����ݸ�˹���ɼ���֪�Ȼ�ѧ����ʽд���µ��Ȼ�ѧ����ʽ����ȷԭ��ء����ع���ԭ�����ܹ���ȷ��д�缫��Ӧʽ��

��ϰ��ϵ�д�
 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д�
�����Ŀ
�����б仯�У���Ҫ������ʵĻ�ԭ������ʵ�ֵ��ǣ�������
| A��H2��HCl |
| B��CO��CO2 |
| C��CuO��Cu |
| D��SO2��SO3 |
��ѧ���ѷ���һ�����������H3������ͬ�����£���������H3��H2��ͬ���ǣ�������
| A���ܶ� | B�������� |
| C�������� | D����� |
 ʯ���ǹ�ҵ��ѪҺ������Ϊ����ɫ�Ľ��ӡ�������Ҫ����Դ��Դ�ͻ���ԭ�ϣ�
ʯ���ǹ�ҵ��ѪҺ������Ϊ����ɫ�Ľ��ӡ�������Ҫ����Դ��Դ�ͻ���ԭ�ϣ�