题目内容
14.下列离子方程式的书写及评价,均合理的是( )| 选项 | 离子方程式 | 评价 |
| A | 将少量的Fe3O4溶解在过量的稀HNO3中Fe3O4+8H+=Fe2++2Fe3++4H2O | 正确,Fe2+与Fe3+物质的量之比为1:2 |
| B | Ba(HCO3)2溶液与足量的NaOH溶液反应Ba2++HCO3 -+OH-═BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
| C | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-═HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
| D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合:2AlO2-+5H+═Al3++Al(OH)3↓+H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2:3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀硝酸能够将亚铁离子氧化成铁离子,离子方程式书写错误;
B.氢氧化钠足量,反应生成碳酸钡沉淀、碳酸钠和水;
C.次氯酸具有强氧化性,能够将亚硫酸氢根离子氧化成硫酸根离子;
D.设溶液体积为1L,偏铝酸钠和HCl的物质的量分别为1mol、2.5mol,1mol偏铝酸钠消耗1molHCl生成1mol氢氧化铝,剩余的1.5molHCl能够溶解0.5mol氢氧化铝,据此判断反应产物及离子方程式.
解答 解:A.Fe3O4与过量的稀HNO3反应,生成的亚铁离子被稀硝酸氧化成了铁离子,正确的离子方程式为:3SO2+2NO3-+3Ba2++2H2O═3BaSO4↓+2NO↑+4H+,故A错误;
B.Ba(HCO3)2溶液与足量的NaOH溶液,反应还生成碳酸根离子,正确的离子方程式为:Ba2++2HCO3-+2OH-═BaCO3↓+2H2O+CO32-,故B错误;
C.过量SO2通入到NaClO溶液中,二者发生氧化还原反应,正确的离子方程式为:ClO-+H2O+SO2═SO42-+2H++Cl-,故C错误;
D.1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合,设溶液体积为1L,偏铝酸钠和HCl的物质的量分别为1mol、2.5mol,1mol偏铝酸钠消耗1molHCl生成1mol氢氧化铝,剩余的1.5molHCl能够溶解0.5mol氢氧化铝,反应的离子方程式为:2AlO2-+5H+═Al3++Al(OH)3↓+H2O,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度中等,明确发生反应实质为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.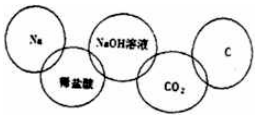 某同学在奥运五连环中填入5种物质 (如图所示),相连环的物质间发生的反应中,没有涉及的基本反应类型是( )
某同学在奥运五连环中填入5种物质 (如图所示),相连环的物质间发生的反应中,没有涉及的基本反应类型是( )
 某同学在奥运五连环中填入5种物质 (如图所示),相连环的物质间发生的反应中,没有涉及的基本反应类型是( )
某同学在奥运五连环中填入5种物质 (如图所示),相连环的物质间发生的反应中,没有涉及的基本反应类型是( )| A. | 分解反应 | B. | 复分解反应 | C. | 化合反应 | D. | 置换反应 |
19.有关氨的说法不正确的( )
| A. | NH3是10电子微粒 | |
| B. | 氨气易液化,液氨可用作制冷剂 | |
| C. | 蘸有浓盐酸的玻璃棒遇氨气产生的白烟 | |
| D. | 氨气是电解质,NH3•H2O是非电解质 |
6.分类是重要的科学研究方法,下列物质分类正确的是( )
| A. | 电解质:胆矾、一水合氨、硫酸钡、CaO | |
| B. | 酸性氧化物:CO2、SO2、NO2、SiO2 | |
| C. | 混合物:铝热剂、干冰、水玻璃、盐酸 | |
| D. | 弱酸:氢碘酸、醋酸、碳酸、次氯酸 |
4.关于几种分子中的化学键描述不正确的是( )
| A. | 苯每个碳原子的未参加杂化的 2p 轨道形成大π键 | |
| B. | CH4中的 4 个 C-H 键都是 H 的 1s 轨道与 C 的 2p 轨道形成的 s-pσ键 | |
| C. | C2H4 中,每个碳原子的 sp2 杂化轨道形成σ键、未杂化的2p 轨道形成π键 | |
| D. | 乙炔分子中,每个碳原子都有两个未杂化的 2p 轨道形成π键 |

 的名称是2,2,4,5-四甲基-3,3-二乙基己烷
的名称是2,2,4,5-四甲基-3,3-二乙基己烷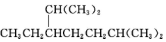 的名称为2,6-二甲基-3-乙基庚烷
的名称为2,6-二甲基-3-乙基庚烷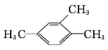 的名称是1,2,4-三甲苯
的名称是1,2,4-三甲苯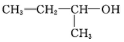 的名称是2-丁醇
的名称是2-丁醇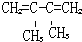 .
.