题目内容
12.下列说法正确的是( )| A. | 冰醋酸、纯碱、明矾、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | 电解质是在水溶液或熔融状态下能导电的化合物 | |
| C. | 在含有1 mol Fe(OH)3的胶体中,含有NA个Fe(OH)3胶粒 | |
| D. | 玻璃棒在化学实验中只起到搅拌的作用 |
分析 A.纯碱是碳酸钠属于盐;
B.电解质是水溶液中或熔融状态下导电的化合物;
C.氢氧化铁胶粒为氢氧化铁的聚集体;
D.过滤操作中玻璃棒的作用是引流.
解答 解:A.纯碱是碳酸钠属于盐,不是碱,故A错误;
B、电解质是水溶液中或熔融状态下导电的化合物,如硫酸钡水溶液中几乎不导电,熔融状态导电是电解质,HCl在溶液中导电是电解质,故B正确;
C.由于氢氧化铁胶粒为氢氧化铁的聚集体,则1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数小于NA,故C错误;
D.过滤操作中玻璃棒的作用是引流,玻璃棒在实验中的作用为搅拌、引流等,故D错误;
故选B.
点评 本题考查了物质分类、电解质概念分析、胶体性质分析应用、仪器的使用,掌握基础是关键,题目较简单,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.大庆市某中学化学实验小组在实验室鉴定某无色溶液.已知溶液中的溶质仅由NH4+、K+、Ag+、Ca2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种组成.取该溶液进行如下实验:
(1)取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
(2)在(1)所得溶液中加入过量NH4HCO3溶液,有气体生成,同时产生白色沉淀甲;
(3)在(2)所得溶液中加入过量Ba(OH)2溶液并加热也有气体生成,同时产生白色沉淀乙
则下列离子在原溶液中一定存在的有( )
(1)取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
(2)在(1)所得溶液中加入过量NH4HCO3溶液,有气体生成,同时产生白色沉淀甲;
(3)在(2)所得溶液中加入过量Ba(OH)2溶液并加热也有气体生成,同时产生白色沉淀乙
则下列离子在原溶液中一定存在的有( )
| A. | K+、CO32、AlO2- | B. | SO42-、AlO2-、K+、CO32-、 | ||
| C. | CO32-、K+、Al3+ | D. | MnO4-、K+、CO32-、NH4+ |
2.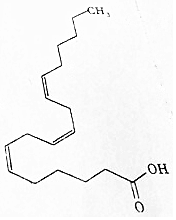 α-亚麻酸是人体必需的重要不饱和脂肪酸,具有增强智力、提高记忆力、保护视力、改善睡眠的作用.其结构简式如图所示,下列相关说法中不正确的是( )
α-亚麻酸是人体必需的重要不饱和脂肪酸,具有增强智力、提高记忆力、保护视力、改善睡眠的作用.其结构简式如图所示,下列相关说法中不正确的是( )
 α-亚麻酸是人体必需的重要不饱和脂肪酸,具有增强智力、提高记忆力、保护视力、改善睡眠的作用.其结构简式如图所示,下列相关说法中不正确的是( )
α-亚麻酸是人体必需的重要不饱和脂肪酸,具有增强智力、提高记忆力、保护视力、改善睡眠的作用.其结构简式如图所示,下列相关说法中不正确的是( )| A. | α-亚麻酸的分子式为C18H30O2 | |
| B. | α-亚麻酸能使酸性高锰酸钾溶液褪色 | |
| C. | α-亚麻酸在一定条件下能发生酯化反应与取代反应 | |
| D. | 1molα-亚麻酸最多能与4molBr2发生加成反应 |
7.下列说法正确的是( )
| A. | SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊试液褪色 | |
| B. | 能使品红溶液褪色的不一定是SO2 | |
| C. | SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同 | |
| D. | 等物质的量的SO2和Cl2相遇在溶液中具有漂白能力 |
4.下列表述正确的是( )
| A. | 比例模型为 ,可以表示甲烷分子,也可以表示四氯化碳分子 ,可以表示甲烷分子,也可以表示四氯化碳分子 | |
| B. | 2CH3CH2OD+O2$→_{△}^{Cu}$2CH3CHO+2DHO | |
| C. | 二氧化硫、氨、煤的液化均为物理变化 | |
| D. | 实验室中制取乙酸乙酯的方程式为CH3COOH+H18O-C2H5CH3COOC2H5+H218O |
2.软锰矿(主要成分是MnO2)与过量KOH和KClO3固体在高温下反应,生成K2MnO4和KCl,其反应化学方程式为 MnO2+KOH+KClO3$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+KCl+H2O(未配平)下列说法中正确的是( )
| A. | 反应中MnO2是氧化剂 | |
| B. | 氧化产物与还原产物物质的量之比为1:3 | |
| C. | KClO3在反应中失去电子 | |
| D. | 反应中每生成l mol K2MnO4,氧化剂得到2 mol电子 |