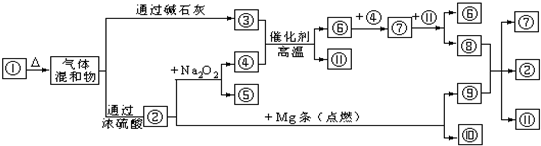
题目内容
下列离子方程式中书写正确的是( )
| A、FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- |
| B、Fe和稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ |
| C、FeCl3溶液与铜 Fe3++Cu═Fe2++Cu2+ |
| D、用醋酸除水垢 2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ |
考点:离子方程式的书写
专题:
分析:A.根据电荷守恒判断,离子方程式两边电荷不守恒;
B.铁与稀硫酸反应生成亚铁离子,不会生成铁离子;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.醋酸能够与碳酸钙反应生成醋酸钙、二氧化碳和水,醋酸和碳酸钙都需要保留化学式.
B.铁与稀硫酸反应生成亚铁离子,不会生成铁离子;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.醋酸能够与碳酸钙反应生成醋酸钙、二氧化碳和水,醋酸和碳酸钙都需要保留化学式.
解答:
解:A.FeCl2溶液中通入Cl2,二者反应生成氯化铁,离子方程式必须满足电荷守恒,正确的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故A错误;
B.铁与稀硫酸反应生成氯化亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.铜与氯化铁反应生成氯化亚铁和氯化铜,离子方程式必须满足电荷守恒,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.醋酸除水垢,水垢的主要成分为碳酸钙,二者反应的离子方程式为:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑,故D正确;
B.铁与稀硫酸反应生成氯化亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.铜与氯化铁反应生成氯化亚铁和氯化铜,离子方程式必须满足电荷守恒,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.醋酸除水垢,水垢的主要成分为碳酸钙,二者反应的离子方程式为:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑,故D正确;
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
某溶液中有NH4+、Mg2+、Fe2+ 和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中大量减少的离子是( )
| A、NH4+、Mg2+ |
| B、Fe2+、Mg2+ |
| C、Fe2+、NH4+ |
| D、Al3+、Fe2+ |
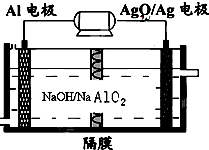 铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示.下列说法正确的是( )
铝电池性能优越,Al-Ag2O电池可用作水下动力电源,其原理如图所示.下列说法正确的是( )| A、电池负极反应式2Ag+2OH--2e-=Ag 2O+H2O |
| B、放电时电池负极附近PH减小 |
| C、电池总反应式2Al+3Ag2O+6H+=2Al3++6Ag+3H2O |
| D、电解液中Na+通过隔膜由右向左移动 |
下列有关化学用语表示正确的是( )
| A、蚁醛的最简式:CH2O | ||
B、中子数为20的氯原子:
| ||
C、氮原子最外层电子轨道表示式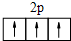 | ||
D、NH4Br的电子式 |
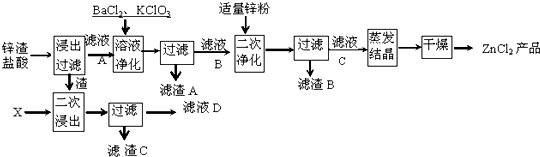
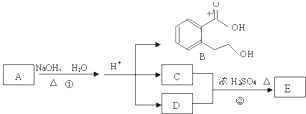 如图中 A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.
如图中 A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.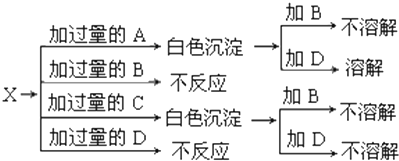 如图中A、B、C、D分别是KNO3、KOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定.
如图中A、B、C、D分别是KNO3、KOH、HNO3和Ba(NO3)2四种溶液中的一种,现利用另一种溶液X,用如图所示的方法可将它们依次确定.