题目内容
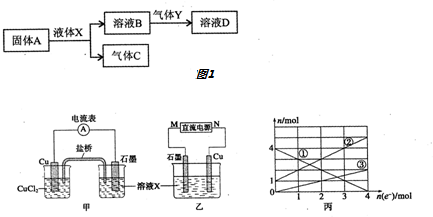
16.25℃时,0.1mol Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
| A. | W点所示的溶液中:c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c(Cl-) | |
| B. | pH=4的溶液中:c(H2CO3)+c(HCO32-)+c(CO32-)<0.1 mol•L-1 | |
| C. | pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3-)═c(OH-)+c(Cl-) | |
| D. | pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3- )>c(H2CO3) |
分析 A.W点溶液中溶质为等物质的量浓度的Na2CO3和NaHCO3,还有溶质NaCl,任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
B.根据图知,pH=4时,c(H2CO3)大于0.02mol/L而小于0.04mol/L,c(HCO3-)=c(CO32-)=0;
C.根据图象可知pH=8时,溶液中c(NaHCO3)远远大于c(Na2CO3),且c(CO32-)=0,这说明反应中恰好是生成碳酸氢钠,溶液中存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断;
D.根据图象可知pH=11时,溶液碳酸钠的浓度远远大于碳酸氢钠,这说明碳酸钠是过量的.
解答 解:A.W点溶液中溶质为等物质的量浓度的Na2CO3和NaHCO3,还有溶质NaCl,任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-),故A错误;
B.根据图知,pH=4时,c(H2CO3)大于0.02mol/L而小于0.04mol/L,c(HCO32-)=c(CO32-)=0,所以溶液中c(H2CO3)+c(HCO32-)+c(CO32-)<0.1 mol•L-1,故B正确;
C.根根据图象可知pH=8时,溶液中c(NaHCO3)远远大于c(Na2CO3),且c(CO32-)=0,这说明反应中恰好是生成碳酸氢钠,溶液中存在电荷守恒和物料守恒,根据物料守恒可知:c(H2CO3)+c(HCO3-)+c(CO32-)=c(Cl-)=$\frac{1}{2}$c(Na+),再结合电荷守恒c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)+c(HCO3-)可得:c(H+)+2c(H2CO3)+2c(HCO3-)=c(OH-)+c(Cl-),故C错误;
D.根据图象可知pH=11时,溶液Na2CO3的浓度远远大于碳酸氢钠,这说明Na2CO3是过量的,加入的HCl量很少,则溶液中c(Cl-)<c(CO32-),故D错误;
故选B.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断能力,明确溶液中溶质成分及其性质是解本题关键,会根据c(NaHCO3)、c(Na2CO3)相对大小确定离子浓度关系,题目难度中等.

| A. | H2O | B. | Na2CO3 | C. | Na2O2 | D. | KOH |
| 选项 | 甲物质 | 乙组中的物质 |
| A | SO2 | KI3溶液、氨水、KMnO4溶液、苯酚钠溶液 |
| B | Mg | Cl2、CO2、NH4Cl溶液、NaOH溶液 |
| C | SiO2 | HF溶液、NaOH溶液、稀硝酸、Na2CO3 |
| D | 稀硫酸 | Al(OH)3、碳、Cu2(OH)2CO3、Cu |
| A. | A | B. | B | C. | C | D. | D |
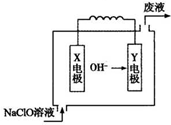
| A. | 镁作Y电极 | |
| B. | 电池工作时Na+向负极移动 | |
| C. | 废液的pH大于NaClO溶液的pH | |
| D. | X电极上发生的反应为:ClO-+2H2O-4e-═ClO3-+4H+ |
| A. | 0.1 mol•L-1 Na2CO3溶液中CO32-、HCO3-和H2CO3总数为0.1 NA | |
| B. | NaCl的沸点为1465℃,1500℃时气体摩尔体积是Vm,此状态下,3Vm L的氯化钠含有3 NA个共价键 | |
| C. | 25℃,1 L pH=1的稀硫酸中含有的H+数为0.1 NA | |
| D. | 1 mol Cu和足量稀硝酸反应产生$\frac{2}{3}$ NA个NO分子 |
| A. | 负极发生的反应为:Fe-2e-═Fe2+ | |
| B. | 正极发生的反应为:2H2O+O2+2e-═4OH- | |
| C. | 钢和铁都是铁合金,所以它们的组成基本相同 | |
| D. | 插在水中的钢柱在水下部分比在空气与水交界处更容易腐蚀 |
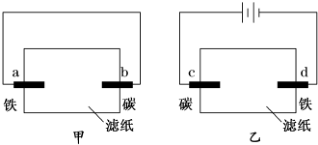
| A. | 滤纸上的阴离子都向碳棒迁移 | B. | a、d两极的电极反应式相同 | ||
| C. | b、d两极附近的溶液都变红 | D. | c、d两极均有少量气体产生 |
 .
. .
.