题目内容
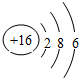
15.A、B、C、D、E是原子序数依次增大的五种短周期元素.A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族元素,B和C的最外层电子数之和与E的最外层电子数相同.A与E形成的化合物化学式为AE,其分子中含18个电子.请回答下列问题:(1)D元素的原子结构示意图为
 .
.(2)由A、B、C三种元素形成的化合物的化学式为NaOH,这种化合物形成的晶体中所含的化学键类型有离子键、共价键.
(3)A、B、D三种元素形成的一种化合物和A、B形成的一种化合物能发生氧化还原反应,反应的化学方程式为H2SO3+H2O2=H2SO4+H2O.
分析 A、B、C、D、E是原子序数依次增大的五种短周期元素,A原子的电子层数与它的核外电子总数相同,则A为H元素;A与E形成的化合物化学式为AE,其分子中含18个电子,故E为Cl元素;A与C同主族,处于ⅠA族,B和C的最外层电子数之和与E的最外层电子数相同,则B的最外层电子数为7-1=6,处于ⅥA族,B与D为同主族,原子序数B小于D,则B为O元素,D为S元素;C原子序数大于氧元素,C与氢元素为同主族,故C为Na元素,据此进行解答.
解答 解:A、B、C、D、E是原子序数依次增大的五种短周期元素,A原子的电子层数与它的核外电子总数相同,则A为H元素;A与E形成的化合物化学式为AE,其分子中含18个电子,故E为Cl元素;A与C同主族,处于ⅠA族,B和C的最外层电子数之和与E的最外层电子数相同,则B的最外层电子数为7-1=6,处于ⅥA族,B与D为同主族,原子序数B小于D,则B为O元素,D为S元素;C原子序数大于氧元素,C与氢元素为同主族,故C为Na元素,
(1)D为硫元素,原子序数为16,其原子结构示意图为: ,
,
故答案为: ;
;
(2)由A、B、C三种元素形成的化合物为氢氧化钠,化学式为:NaOH,氢氧化钠是离子化合物,由钠离子与氢氧根离子构成,电子式为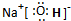 ,晶体中钠离子与氢氧根离子之间形成离子键,氢氧根离子中氢原子与氧原子之间形成共价键,
,晶体中钠离子与氢氧根离子之间形成离子键,氢氧根离子中氢原子与氧原子之间形成共价键,
故答案为:NaOH;离子键、共价键;
(3)由A、B、D三种元素形成的一种化合物和A、B两种元素形成的一种化合物能发生氧化还原反应,应是亚硫酸与过氧化氢反应生成硫酸与水,反应的化学方程式:H2SO3+H2O2=H2SO4+H2O,
故答案为:H2SO3+H2O2=H2SO4+H2O.
点评 本题考查结构性质位置关系应用,题目难度中等,涉及元素推断及元素化合物性质、常用化学用语等知识,推断元素是解题关键,注意掌握元素周期表结构、元素周期律内容.

| A. | X的最高价氧化物对应的水化物是弱酸 | |
| B. | Z位于元素周期表的第3周期第ⅥA族 | |
| C. | Y的最高氧化物对应的水化物能溶于NaOH溶液 | |
| D. | 原子半径的大小顺序:r(Z)>r(Y)>r(X) |
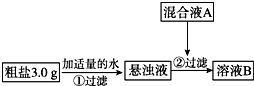 目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(如图称为粗盐)(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.
目前国内外使用的融雪剂一般有两大类:一类是以醋酸钾为主要成分的有机融雪剂;另一类是以“氯盐”为主要成分的无机融雪剂,如氯化钠、氯化钙、氯化镁等,通称“化冰盐”.某研究性学习小组拟对融雪氯盐(如图称为粗盐)(主要含有氯化钠及不溶性杂质、Mg2+、Ca2+等)进行回收提纯研究.| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 6.8×10-8 | 4.0×10-9 | 1.8×10-11 |
(1)加入混合液A的主要成分是NaOH、Na2CO3 (填化学式).
(2)为检验溶液B中的Mg2+、Ca2+,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+,向其中一支试管中加入NaOH溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+,向另一支试管中加入某溶液,看是否有沉淀生成.下列三种溶液,其沉淀效果最好的是A.
A.0.1mol•L-1 Na2CO3溶液
B.0.1mol•L-1 Na2SO3溶液
C.0.1mol•L-1 Na2C2O4溶液
(3)在除杂过程中,向粗盐悬浊液中加混合液A时需控制溶液pH=12以确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在1.8×10-7mol•L-1以下.
(4)对溶液B加热并不断滴加6mol•L-1的盐酸,同时用pH试纸检测溶液,直至pH=2时停止加盐酸,得到溶液C.该操作的目的是除去NaOH和Na2CO3.
(5)溶液C倒入蒸发皿中,加热蒸发并不断搅拌,直到有大量固体析出时停止加热.
(6)足量CaCO3固体分别加入:①30mL水 ②10mL 0.2mol/LNa2CO3溶液 ③50mL 0.01mol/L氯化钙溶液 ④100mL 0.01mol/L盐酸中溶解至溶液饱和.
请确定各溶液中Ca2+的浓度由大到小的顺序为:③④①②.
| A. | SO2 | B. | H2SiO3 | C. | CuCl2 | D. | Fe﹙OH﹚3 |
| A. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 实验时手指不小心沾上苯酚,立即用70℃以上的热水清洗 | |
| D. | 实验室检验卤代烃时,试剂只需用NaOH的水溶液和AgNO3溶液即可 |
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| B. | CH2=CH2+Br2→BrCH2CH2Br | |
| C. | CH3CH2CH2Cl+NaOH $→_{△}^{酸}$CH3CH=CH+NaCl+H2O | |
| D. | 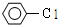 +H2O$→_{△}^{酸}$ +H2O$→_{△}^{酸}$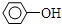 +HCl +HCl |
| A. | 钠与CuSO4溶液反应:2Na+Cu=Cu↓+2Na+ | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| A. | 负极反应为:14H2O+7O2+28e-=28OH- | |
| B. | 放电一段时间后,负极周围的pH升高 | |
| C. | 放电过程中OH-向正极移动 | |
| D. | 每消耗1mol C2H6,则电路上转移的电子为14mol |
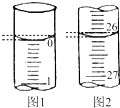 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液(盛放于锥形瓶中)时,选择酚酞作指示剂,请填写下列空白:(1)滴定时一般左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶,直到加入最后一滴盐酸,溶液溶液颜色由红色变为无色,且半分钟内不变色,即达到滴定终点.若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用盐酸的体积为26.10 mL.
(2)某学生重复三次实验,记录数据如下表所示(待测NaOH溶液的体积均为25.00mL);
| 滴定次数 | 0.1000mol-L-1盐酸的体积/mL | ||
| 滴定前 | 滴定后 | 体积/mL | |
| 1 | 0.10 | 26.21 | 26.11 |
| 2 | 1.56 | 31.30 | 29.74 |
| 3 | 0.22 | 26.31 | 26.09 |
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏高的是AC.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管尖嘴处在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定开始时仰视读数,滴定结束时俯视读数.