题目内容
下列说法正确的是( )
A、CH4(g)+
| ||
| B、在25℃、101kPa,1mol硫和2mol硫的燃烧热相等 | ||
| C、CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 | ||
| D、101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
考点:燃烧热,反应热和焓变
专题:化学反应中的能量变化
分析:A.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量;
B.条件一定,燃烧热为定值,与物质的量无关;
C.燃烧反应为放热反应;
D.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,产物为稳定氧化物以此解答该题.
B.条件一定,燃烧热为定值,与物质的量无关;
C.燃烧反应为放热反应;
D.燃烧热是指1mol纯净物完全燃烧生成稳定的氧化物放出的热量,产物为稳定氧化物以此解答该题.
解答:
解:A.产物CO不是稳定氧化物,△H不代表燃烧热,故A错误;
B.条件一定,燃烧热为定值,与物质的量无关,故B正确;
C.CO的燃烧反应一定是放热反应,故C错误;
D.101kPa时,1mol碳完全燃烧生成二氧化碳,所放出的热量为碳的燃烧热,故D错误;
故选:B.
B.条件一定,燃烧热为定值,与物质的量无关,故B正确;
C.CO的燃烧反应一定是放热反应,故C错误;
D.101kPa时,1mol碳完全燃烧生成二氧化碳,所放出的热量为碳的燃烧热,故D错误;
故选:B.
点评:本题考查了燃烧热的概念.表示燃烧热的热化学方程式中可燃物为1mol,产物为稳定氧化物,题目难度不大.

练习册系列答案
相关题目
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、HCO3-、C1-、K+ |
| C、Fe3+、K+、I-、H+ |
| D、H+、Cl-、Na+、CO32- |
下列关于溶液的说法中,正确的是( )
| A、凡是均一、稳定的液体,就是溶液 |
| B、长期放置后不会分层的液体,就是溶液 |
| C、一种物质里分散着另一种物质的液体是溶液 |
| D、溶液一定是均一、稳定的混合物 |
用下列装置进行相应实验,能达到实验目的是( )
A、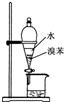 用如图所示装置分离出溴苯 |
B、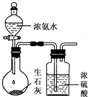 用如图所示装置制取干燥的氨气 |
C、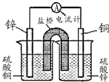 用如图设计成铜锌原电池装置 |
D、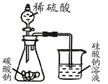 用如图证明氢化物稳定性SiH4>CH4>H2S |
下列有关实验的说法正确的是( )
A、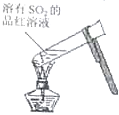 加热后溶液的颜色变为无色 |
B、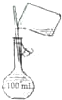 配置100mL0.01moL/L 溶液 |
C、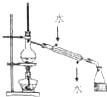 实验室用该装置制取蒸馏水 |
D、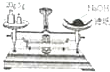 称量25克 |
下列关于胶体的说法中正确的是( )
| A、胶体外观不均匀 |
| B、胶体粒子能通过半透膜 |
| C、胶体不稳定,静置后容易产生沉淀 |
| D、胶体微粒做不停的无秩序运动 |
某无色溶液能和Al反应放出H2,在该溶液中可能大量共存的离子组是( )
| A、Fe2+、NO3-、Cl-、H+ |
| B、Na+、OH-、NO3-、Cl- |
| C、Na+、SO42-、HCO3-、K+ |
| D、H+、SO42-、Cl-、Fe3+ |
已知25℃下,醋酸溶液中各微粒存在下述关系:K=1.75×10-5下列有关说法可能成立的是( )
| A、25℃条件下,向该溶液中加入一定量的盐酸时,K=8×10-5 |
| B、25℃条件下,向该溶液中加入一定量的盐酸时,K=2×10-4 |
| C、标准状况下,醋酸溶液中K=1.75×10-5 |
| D、升高到一定温度,K=7.2×10-5 |