题目内容
3.阿伏加德罗常数的值为NA.下列说法正确的是( )| A. | 2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子 | |
| B. | 0.1mol的11B中,含有0.6NA 个中子 | |
| C. | 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA | |
| D. | 常温常压下,17g 羟基含有的电子总数为 7 NA |
分析 A、标况下苯为液体;
B、11B中含6个中子;
C、求出混合气体的物质的量,然后根据分子个数N=nNA来计算;
D、求出羟基的物质的量,然后根据羟基中含9个电子来分析.
解答 解:A、标况下苯为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、11B中含6个中子,故0.1mol11B中含0.6mol即0.6NA个中子,故B正确;
C、标况下2.24L混合气体的物质的量为0.1mol,故分子个数N=nNA=0.1NA个,故C错误;
D、17g羟基的物质的量为1mol,而羟基中含9个电子,故1mol羟基中含9NA个电子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
14.下列物质中,既能发生取代反应,又能发生消去反应,同时催化氧化生成醛的是( )
| A. |  | B. |  | ||
| C. | CH3OH | D. |  |
15.下列离子或分子能够在指定的分散系中大量共存的是( )
| A. | 空气中:SO2、NO、N2、NH3 | |
| B. | 明矾溶液中:Na+、K+、CH3COO-、HCO3- | |
| C. | 过量铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 常温下,水电离出的c(H+)=1×10-12mol/L的溶液中:Ba2+、Na+、Cl-、NO3- |
18.如图是产生和收集气体的实验装置,该装置最适合于( )


| A. | 用浓硝酸与Cu 反应制取NO2 | B. | 用浓盐酸和 MnO2 反应制取 C12 | ||
| C. | 用 NH4Cl 和 Ca(OH)2 反应制取 NH3 | D. | 用 H2O2溶液和 MnO2 反应制取 O2 |
8.金属冶炼中不会涉及到的反应类型是( )
| A. | 氧化还原反应 | B. | 置换反应 | C. | 热分解反应 | D. | 复分解反应 |
15.在恒温恒容条件下,能使A(g)+2B(g)?C(g)+D(g)正反应速率增大的措施是( )
| A. | 减小C 的浓度 | B. | 通入He气使压强增大 | ||
| C. | 减小B的浓度 | D. | 增大A或B的浓度 |
12.把a mol H2和b mol C2H4混合,在一定条件下使它们一部分发生反应生成w molC2H6,将反应混合气体完全燃烧,余下的C2H4消耗氧气的物质的量为( )
| A. | a+3b | B. | $\frac{a}{2}$+3b | C. | $\frac{a}{2}$+3b+$\frac{7}{2}$ w | D. | 3(b-w) |
13.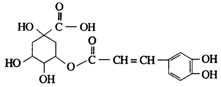 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
 金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )
金银花中含有绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法不正确的是( )| A. | 绿原酸的分子式为C16H8O9 | |
| B. | 1个绿原酸分子中含有4个手性碳原子 | |
| C. | 1mol绿原酸最多与4molNaOH反应 | |
| D. | 1mol绿原酸最多能与6molH2发生反应 |



 .
. .
. 有多种同分异构体,试写出所有苯环上含有1个醛基和2个羟基,且核磁共振氢谱显示为4组峰的芳香族化合物的结构简式
有多种同分异构体,试写出所有苯环上含有1个醛基和2个羟基,且核磁共振氢谱显示为4组峰的芳香族化合物的结构简式 .
.