题目内容
25℃时,将0.02mol CH3COONa和0.01mol HCl溶于水,配成1L混合溶液:
(1)写出该溶液中溶质的电离平衡式和水解离子方程式:
① ;
② ;
(2)若pH=4.7溶液中的离子浓度大小关系是
(3)在这些粒子中,浓度为0.01mol?L-1的是 ,
(4)加入适量NaOH固体,当pH=7时,溶液中c(Na+)═ .
(1)写出该溶液中溶质的电离平衡式和水解离子方程式:
①
②
(2)若pH=4.7溶液中的离子浓度大小关系是
(3)在这些粒子中,浓度为0.01mol?L-1的是
(4)加入适量NaOH固体,当pH=7时,溶液中c(Na+)═
考点:电离方程式的书写,离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:将0.02mol CH3COONa和0.01mol HCl溶于水,配成1L混合溶液,反应后溶液的溶质为CH3COOH、CH3COONa、NaCl,物质的量浓度分别为0.01mol/L,0.01mol/L,0.01mol/L,
(1)①溶液中存在醋酸的电离平衡;
②溶液中存在醋酸钠的水解平衡;
(2)若pH=4.7溶液中,醋酸的电离程度大于醋酸根离子的水解程度;
(3)根据溶质的浓度判断;
(4)根据溶液中的电荷守恒分析.
(1)①溶液中存在醋酸的电离平衡;
②溶液中存在醋酸钠的水解平衡;
(2)若pH=4.7溶液中,醋酸的电离程度大于醋酸根离子的水解程度;
(3)根据溶质的浓度判断;
(4)根据溶液中的电荷守恒分析.
解答:
解:将0.02mol CH3COONa和0.01mol HCl溶于水,配成1L混合溶液,反应后溶液的溶质为CH3COOH、CH3COONa、NaCl,物质的量浓度分别为0.01mol/L,0.01mol/L,0.01mol/L,
(1)①溶液中存在醋酸的电离平衡,其电离方程式为:CH3COOH?CH3COO-+H+,
故答案为:CH3COOH?CH3COO-+H+;
②溶液中存在醋酸钠的水解平衡,醋酸根离子水解生成醋酸和氢氧根离子,其水解方程式为:CH3COO?+H2O?CH3COOH+OH?;
故答案为:CH3COO?+H2O?CH3COOH+OH?;
(2)若pH=4.7溶液中,醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COO?)>0.01mol/L,氯离子不水解,则c(Cl-)=0.01mol/L,则离子浓度大小关系是c(Na+)>c(CH3COO?)>c(Cl-)>c(H+)>c(OH-);
故答案为:c(Na+)>c(CH3COO?)>c(Cl-)>c(H+)>c(OH-);
(3)反应后溶液的溶质为CH3COOH、CH3COONa、NaCl,物质的量浓度分别为0.01mol/L,0.01mol/L,0.01mol/L,其中氯离子不水解,其浓度为c(Cl-)=0.01mol/L,
故答案为:Cl-;
(4)加入适量NaOH固体,当pH=7时,溶液中的电荷守恒为:c(Na+)+c(H+)=c(CH3COO?)+c(Cl-)+c(OH-),pH=7,则c(H+)=c(OH-),
所以c(Na+)=c(CH3COO?)+c(Cl-);
故答案为:c(CH3COO?)+c(Cl-).
(1)①溶液中存在醋酸的电离平衡,其电离方程式为:CH3COOH?CH3COO-+H+,
故答案为:CH3COOH?CH3COO-+H+;
②溶液中存在醋酸钠的水解平衡,醋酸根离子水解生成醋酸和氢氧根离子,其水解方程式为:CH3COO?+H2O?CH3COOH+OH?;
故答案为:CH3COO?+H2O?CH3COOH+OH?;
(2)若pH=4.7溶液中,醋酸的电离程度大于醋酸根离子的水解程度,则c(CH3COO?)>0.01mol/L,氯离子不水解,则c(Cl-)=0.01mol/L,则离子浓度大小关系是c(Na+)>c(CH3COO?)>c(Cl-)>c(H+)>c(OH-);
故答案为:c(Na+)>c(CH3COO?)>c(Cl-)>c(H+)>c(OH-);
(3)反应后溶液的溶质为CH3COOH、CH3COONa、NaCl,物质的量浓度分别为0.01mol/L,0.01mol/L,0.01mol/L,其中氯离子不水解,其浓度为c(Cl-)=0.01mol/L,
故答案为:Cl-;
(4)加入适量NaOH固体,当pH=7时,溶液中的电荷守恒为:c(Na+)+c(H+)=c(CH3COO?)+c(Cl-)+c(OH-),pH=7,则c(H+)=c(OH-),
所以c(Na+)=c(CH3COO?)+c(Cl-);
故答案为:c(CH3COO?)+c(Cl-).
点评:本题考查了弱电解质的电离和盐的水解、离子浓度大小比较等,侧重于考查学生对基础知识的应用能力,题目难度中等,注意把握溶液中的守恒关系.

练习册系列答案
相关题目
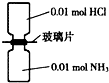 NA表示阿伏加德罗常数的值,常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是( )
NA表示阿伏加德罗常数的值,常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应.下列说法正确的是( )| A、反应前气体的总体积为0.448L |
| B、生成物中含有0.01NA个分子 |
| C、装置中氢元素的总质量为0.04g |
| D、生成物完全溶于水后所得溶液含有0.01NA个NH4+ |
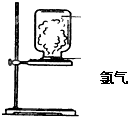 如图,取一块黄豆大小的金属钠放在石棉网上,用酒精灯预热,待钠熔成球状时,将盛氯气的集气瓶倒扣在钠的上方,钠会在氯气中剧烈燃烧,产生大量白烟,请回答下列问题:
如图,取一块黄豆大小的金属钠放在石棉网上,用酒精灯预热,待钠熔成球状时,将盛氯气的集气瓶倒扣在钠的上方,钠会在氯气中剧烈燃烧,产生大量白烟,请回答下列问题: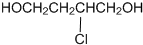
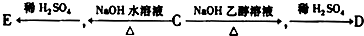
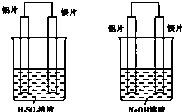 有甲和乙两位同学均想利用原电池反应来检测金属的活动性顺序,两人都使用镁片和铝片作电极,但甲同学将电极放到6mol?L-1 H2SO4溶液中,乙同学将电极放到6mol?L-1NaOH溶液中,如图所示:
有甲和乙两位同学均想利用原电池反应来检测金属的活动性顺序,两人都使用镁片和铝片作电极,但甲同学将电极放到6mol?L-1 H2SO4溶液中,乙同学将电极放到6mol?L-1NaOH溶液中,如图所示: