题目内容
将0.2mol?L-1 NaHCO3溶液与0.1mol?L-1 KOH溶液等体积混合,下列关系正确的是( )
| A、2c(K+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
| B、c(Na+)>c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| C、c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.1mol?L-1 |
| D、3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:将0.2mol?L-1NaHCO3溶液与0.1mol?L-1KOH溶液等体积混合,反应后的溶质为0.025mol/L的碳酸钾、碳酸钠和0.05mol/L的NaHCO3,碳酸根离子的水解程度大于碳酸氢根离子,则溶液中碳酸氢根离子浓度大于0.05mol/L,碳酸根离子浓度小于0.05mol/L;钾离子浓度为0.05mol/L、钠离子浓度为0.1mol/L,溶液显示碱性,则c(OH-)>c(H+),然后结合电荷守恒、物料守恒对各选项进行判断.
解答:
解:0.2mol?L-1NaHCO3溶液与0.1mol?L-1KOH溶液等体积混合,反应后的溶质为0.025mol/L的碳酸钾、碳酸钠和0.05mol/L的NaHCO3,
A.混合液中钾离子浓度为0.05mol/L,则2c(K+)=0.1mol/L,根据物料守恒可得:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L,则c(HCO3-)+2c(CO32-)+c(H2CO3)>0.1mol/L,所以2c(K+)<c(HCO3-)+2c(CO32-)+c(H2CO3),故A错误;
B.由于碳酸氢根离子、碳酸根离子水解,则溶液显示碱性,c(OH-)>c(H+);碳酸根离子的水解程度大于碳酸氢根离子,则溶液中碳酸氢根离子浓度大于0.05mol/L,碳酸根离子浓度小于0.05mol/L;钾离子浓度为0.05mol/L、钠离子浓度为0.1mol/L,则溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(K+)>c(CO32-)>c(OH-)>c(H+),故B错误;
C.根据物料守恒可得:①c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L=c(Na+)=0.1mol/L、②c(K+)=0.05,根据电荷守恒可得:③c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(K+)+c(Na+),根据①③可得:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+c(K+),由于c(K+)=0.05,则c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.05mol?L-1,故C错误;
D.根据电荷守恒可得:c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(K+)+c(Na+),由于混合液中c(Na+)=0.1mol/L、c(K+)=0.05,则c(Na+)=2c(K+),所以3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D正确;
故选D.
A.混合液中钾离子浓度为0.05mol/L,则2c(K+)=0.1mol/L,根据物料守恒可得:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L,则c(HCO3-)+2c(CO32-)+c(H2CO3)>0.1mol/L,所以2c(K+)<c(HCO3-)+2c(CO32-)+c(H2CO3),故A错误;
B.由于碳酸氢根离子、碳酸根离子水解,则溶液显示碱性,c(OH-)>c(H+);碳酸根离子的水解程度大于碳酸氢根离子,则溶液中碳酸氢根离子浓度大于0.05mol/L,碳酸根离子浓度小于0.05mol/L;钾离子浓度为0.05mol/L、钠离子浓度为0.1mol/L,则溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(K+)>c(CO32-)>c(OH-)>c(H+),故B错误;
C.根据物料守恒可得:①c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L=c(Na+)=0.1mol/L、②c(K+)=0.05,根据电荷守恒可得:③c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(K+)+c(Na+),根据①③可得:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+c(K+),由于c(K+)=0.05,则c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.05mol?L-1,故C错误;
D.根据电荷守恒可得:c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(K+)+c(Na+),由于混合液中c(Na+)=0.1mol/L、c(K+)=0.05,则c(Na+)=2c(K+),所以3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D正确;
故选D.
点评:本题考查了溶液中离子浓度大小比较、酸碱混合的定性判断,题目难度较大,正确分析混合液中的溶质组成为解答关键,注意掌握判断溶液中离子浓度大小的方法,选项C为易错点,需要明确混合液体积比原溶液体积扩大了1倍,则钾离子浓度减小为原先的一半.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在给定条件的水溶液中能大量共存的粒子组是( )
| A、无色透明的溶液:Fe3+、K+、OH-、NO3- |
| B、与Al反应生成H2的溶液:Na+、Ma2+、NO3-、HCO3- |
| C、c(OH-)=1mol/L的溶液:K+、Ca2+、Cl-、H2SO3 |
| D、CH3COOH:SO42-、Cl-、Cu2+、NH4+ |
下列说法中不正确的是( )
| A、溶解度:Na2CO3大于NaHCO3 |
| B、稳定性:Na2CO3大于NaHCO3 |
| C、与酸反应剧烈程度:NaHCO3大于Na2CO3 |
| D、石灰水可与Na2CO3反应而不与NaHCO3反应 |
常温下,将Na2CO3和NaHCO3混合物〔
=a a≤3〕溶于水制得稀溶液,下列有关该溶液中微粒的物质的量浓度关系正确的是( )
| n(Na2CO3) |
| n(NaHCO3) |
| A、a=1则c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| B、a=2则c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C、a为任意值时,则c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、a=0则c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
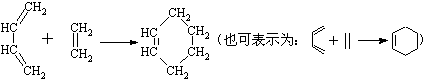

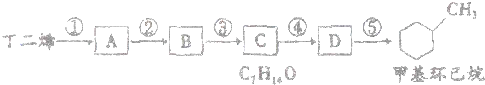
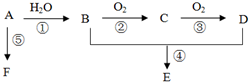 已知A是一种相对分子质量为28的气态烃,它可转化为其他常见有机物,转化关系如图所示.
已知A是一种相对分子质量为28的气态烃,它可转化为其他常见有机物,转化关系如图所示.