题目内容
19.以溴乙烷为原料制备1,2─二溴乙烷(反应条件略去),方案中最合理的是( )| A. | CH3CH2Br→CH3CH2OH→CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br→CH2=CH2 $\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br→CH2=CH2 $\stackrel{Br_{2}}{→}$CH2BrCH2Br |
分析 溴乙烷含有溴原子,可在氢氧化钠水溶液中发生水解反应,在氢氧化钠醇溶液中发生消去反应,应先发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,要考虑到反应原理是否正确外,还要考虑到对环境是否造成污染,以及生产成本问题,以此解答该题.
解答 解:A.溴乙烷在氢氧化钠醇溶液加热条件下直接生成烯,原理复杂,故A不选;
B.溴乙烷与溴发生取代反应,不能制备纯净的1,2-二溴乙烷,故B不选;
C.溴乙烷与溴发生取代反应,不能制备纯净的1,2-二溴乙烷,故C不选;
D.溴乙烷在氢氧化钠醇溶液、加热条件下发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2二溴乙烷,原理正确,不存在其它副产物,故D选;
故选D.
点评 本题考查有机物的合成,为高考中的常见题型,属于中等难度的试题,有利于拓展学生的视野,开阔学生的思维,提高学生的学习效率,题目难度中等.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
9.下列根据实验操作和实验现象所得出的结论,正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱 和Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生 变性 |
| B | 在CuSO4溶液中加入KI溶液,再 加入苯,振荡后静置 | 有白色沉淀生成,苯层 呈紫红色 | 白色沉淀可能 为CuI |
| C | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
| D | 将Fe(NO3)2样品溶于稀H2SO4后, 滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2样品 已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
10.常温下,下列物质能用铝制器皿盛放的是( )
| A. | 稀硫酸 | B. | 氢氧化钠溶液 | C. | 稀硝酸 | D. | 浓硝酸 |
7.下列不能证明Cl元素的非金属性强于S元素的是( )
| A. | HCl的稳定性强于H2S | |
| B. | Cl元素最高正价为+7,而S元素最高正价为+6 | |
| C. | 将Cl2通入Na2S溶液中,产生黄色沉淀 | |
| D. | 单质与H2化合所需的反应条件,S比Cl2苛刻 |
14.如图有机物X是一种医药中间体,下列有关这个化合物的说法正确的是( )


| A. | 化合物X的分子式是C16H11O4 | |
| B. | 不能与饱和Na2CO3溶液反应 | |
| C. | 化合物X可由 和 和  通过酯化反应得到 通过酯化反应得到 | |
| D. | 1 mol化合物X最多能与3 mol NaOH反应 |
10.药物阿司匹林可由水杨酸制得,它们的结构如图所示.有关说法正确的是( )


| A. | 在核磁共振氢谱中水杨酸与阿司匹林应该分别为6个吸收峰与8个吸收峰 | |
| B. | 阿司匹林的分子式为C9H10O4 | |
| C. | 水杨酸可以发生取代反应、加成反应、氧化反应和水解反应 | |
| D. | 1 mol阿司匹林最多可消耗3 mol NaOH或1 mol NaHCO3 |
7.海带是一种富含生物碘的海洋植物,碘是人体必需的微量元素,人体内碘的含量直接影响身体健康,为了防止缺碘,通常向食盐中加入碘酸钾(KIO3),以补充人体对碘的需求.各物质的密度、沸点如下表所示,图1为某兴趣小组从海带中提取碘单质的过程.
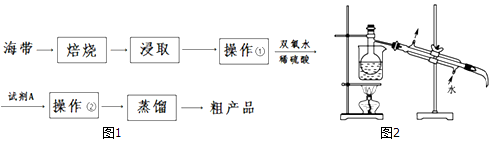
回答下列问题:
(1)实验室焙烧海带时,用不到的仪器有CE (填选项字母).
A.泥三角 B.三脚架 C.烧杯 D.坩埚 E.蒸发皿 F.酒精灯
(2)向浸取液中加入足量的双氧水和稀硫酸时,发生反应的离子方程式为2I-+H2O2+2H+═I2+2H2O.
(3)操作①中除用到玻璃棒外,还需要的玻璃仪器有烧杯、漏斗.
(4)试剂A的名称为四氯化碳 (从上表给出的试剂中选择).
(5)图2是进行蒸馏时的部分仪器,图中缺少的玻璃仪器的名称是温度计、锥形瓶.
(6)工业上可用碘制取碘酸钾,其反应为I2+2KClO3═2KIO3+Cl2↑,下列有关叙述不正确的是A (填选项字母).
A.氧化性:I2>Cl2
B.每生成1mol KIO3,转移5mol e-
C.该反应是置换反应
D.反应物和生成物中均含有共价键.
| 物质 | 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) |
| 密度/g•cm-3 | 0.789 | 1.595 | 0.71~0.76 | 4.93 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |

回答下列问题:
(1)实验室焙烧海带时,用不到的仪器有CE (填选项字母).
A.泥三角 B.三脚架 C.烧杯 D.坩埚 E.蒸发皿 F.酒精灯
(2)向浸取液中加入足量的双氧水和稀硫酸时,发生反应的离子方程式为2I-+H2O2+2H+═I2+2H2O.
(3)操作①中除用到玻璃棒外,还需要的玻璃仪器有烧杯、漏斗.
(4)试剂A的名称为四氯化碳 (从上表给出的试剂中选择).
(5)图2是进行蒸馏时的部分仪器,图中缺少的玻璃仪器的名称是温度计、锥形瓶.
(6)工业上可用碘制取碘酸钾,其反应为I2+2KClO3═2KIO3+Cl2↑,下列有关叙述不正确的是A (填选项字母).
A.氧化性:I2>Cl2
B.每生成1mol KIO3,转移5mol e-
C.该反应是置换反应
D.反应物和生成物中均含有共价键.
10.下列物质中,只含离子键的是( )
| A. | H2 | B. | NH3 | C. | MgCl2 | D. | NaOH |