题目内容
8.下列说法正确的是( )| A. | 反应N2 (g)+3H2 (g)?2NH3 (g)的△H<0,△S>0 | |
| B. | 地下钢铁管道用导线连接锌块可以减缓管道的腐蚀 | |
| C. | 常温下,Ksp[Mg(OH)2]=5.6×10-12,pH=10的含Mg2+溶液中,c(Mg2+ )≤5.6×10-4 mol•L-1 | |
| D. | 常温常压下,锌与稀H2SO4反应生成11.2 L H2,反应中转移的电子数为6.02×1023 |
分析 A.由化学计量数可知△S<0;
B.导线连接锌块,构成原电池时Zn为负极;
C.pH=10的含Mg2+溶液中,c(OH-)=10-4 mol•L-1,c(Mg2+ )≤$\frac{Ksp}{c(O{H}^{-})^{2}}$;
D.常温常压下,Vm≠22.4L/mol.
解答 解:A.合成氨反应为放热反应,△H<0,且为气体体积减小的反应,则△S<0,故A错误;
B..导线连接锌块,构成原电池时Zn为负极,Fe作正极被保护,则可以减缓管道的腐蚀,故B正确;
C.pH=10的含Mg2+溶液中,c(OH-)=10-4 mol•L-1,c(Mg2+ )≤$\frac{5.6×1{0}^{-12}}{(1{0}^{-4})^{2}}$=5.6×10-4 mol•L-1,故C正确;
D.常温常压下,Vm≠22.4L/mol,则不能利用氢气的体积计算物质的量及转移电子数,故D错误;
故选BC.
点评 本题考查较综合,涉及反应热与焓变、原电池、难溶电解质Ksp的计算等,为高频考点,把握化学反应原理为解答的关键,侧重分析能力和应用能力的考查,注意选项D为易错点,题目难度中等.

练习册系列答案
相关题目
13. 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )| A. | 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4 | |
| B. | 电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g | |
| C. | 石墨烯的作用主要是提高电极a的导电性 | |
| D. | 电池充电时间越长,电池中的Li2S2量越多 |
8.常温下,Ka (HCOOH)=1.77×10-4,Ka (CH3COOH)=1.75×10-5,Kb (NH3•H2O)=1.76×10-5,下列说法正确的是( )
| A. | 浓度均为0.1 mol•L-1的 HCOONa和NH4Cl 溶液中阳离子的物质的量浓度之和:前者大于后者 | |
| B. | 用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积相等 | |
| C. | 0.2 mol•L-1 HCOOH 与 0.1 mol•L-1 NaOH 等体积混合后的溶液中:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+) | |
| D. | 0.2 mol•L-1 CH3COONa 与 0.1 mol•L-1盐酸等体积混合后的溶液中(pH<7):c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
16.下列说法正确的是( )
| A. | HOCH2CH=CH2能发生取代反应,加成反应、氧化反应 | |
| B. | 月桂烯(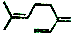 )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 | |
| C. | 甲烷、乙烯、苯和乙醇都能使酸性KMnO4溶液褪色 | |
| D. | 油脂皂化反应得到高级脂肪酸与甘油 |
3.下列有关物质的性质与用途具有对应关系的是( )
| A. | 活性炭具有还原性,可用作冰箱除味剂 | |
| B. | 二氧化硫具有氧化性,可用作造纸漂白剂 | |
| C. | Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 | |
| D. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
2.W、X、Y、Z、M、N六种主族元素,它们在周期表中位置如图所示,下列说法正确的是( )
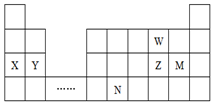

| A. | 原子半径:Y>Z>W,简单离子半径:M->Z2->W2- | |
| B. | 单质的还原性:X>Y,简单氢化物的沸点:Z>W | |
| C. | 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强 | |
| D. | 元素N位于金属与非金属的分界线附近,可以推断N的单质可作 半导体材料 |
3.利用H2和O2制备H2O2的原理为①H2(g)+A(1)?B(1)△H1 ②O2(g)+B(1)?A(1)+H2O2(1)△H2巳知:A、B均为有机物,两个反应均能自发进行,下列说法正确的是( )
| A. | △H2>0 | |
| B. | B为H2和O2制备H2O2的催化剂 | |
| C. | 反应①的正反应的活化能大于逆反应的活化能 | |
| D. | H2(g)+O2(g)?H2O2(1)的△H<0 |
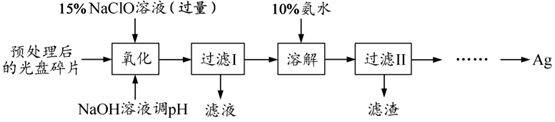
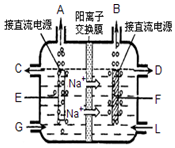 食盐是日常生活必需品,也是重要的化工原料.
食盐是日常生活必需品,也是重要的化工原料.