题目内容
现有失去标签的CaCl2、AgNO3、HCl和Na2CO3四瓶溶液.为了确定这四种溶液成分,将他们编号为A、B、C、D后进行化学实验.实验记录如下:
根据上述实验填空:
(1)A、B、C三瓶溶液分别是(用化学式表示): 、 、 .
(2)写出B和D反应的离子方程式: .
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 无现象 |
| ② | B+D | 有气体放出 |
| ③ | C+B | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
(1)A、B、C三瓶溶液分别是(用化学式表示):
(2)写出B和D反应的离子方程式:
考点:无机物的推断,物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:HCl和Na2CO3反应生成气体,AgNO3分别与CaCl2、HCl和Na2CO3反应均生成沉淀,且CaCl2、AgNO3、HCl都能与Na2CO3反应,结合实验中B+D反应生成气体,A+D反应生成沉淀,A+B无现象,则B为HCl,D为Na2CO3,所以A为CaCl2,C为AgNO3,再结合物质的性质及发生的反应来解答.
解答:
解:HCl和Na2CO3反应生成气体,AgNO3分别与CaCl2、HCl和Na2CO3反应均生成沉淀,且CaCl2、AgNO3、HCl都能与Na2CO3反应,结合实验中B+D反应生成气体,A+D反应生成沉淀,A+B无现象,则B为HCl,D为Na2CO3,所以A为CaCl2,C为AgNO3,
(1)由上述分析可知,A为CaCl2,B为HCl,C为AgNO3,故答案为:CaCl2;HCl;AgNO3;
(2)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,离子反应为2H++CO32-=CO2↑+H2O,故答案为:2H++CO32-=CO2↑+H2O.
(1)由上述分析可知,A为CaCl2,B为HCl,C为AgNO3,故答案为:CaCl2;HCl;AgNO3;
(2)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,离子反应为2H++CO32-=CO2↑+H2O,故答案为:2H++CO32-=CO2↑+H2O.
点评:本题考查无机物的推断,为高频考点,明确物质之间的反应是解答本题的关键,注意碳酸钠能与其他三种物质反应,硝酸银也能与其他三种物质反应,题目难度中等.

练习册系列答案
相关题目
下列说法中正确的是.
| A、1molH2SO4与1molBa(OH)2完全中和所放出的热量为中和热 |
| B、中和反应都是放热反应 |
| C、氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量高 |
| D、CO燃烧是吸热反应 |
二氧化硫是污染大气的有害物质之一.下列情况,不是空气中二氧化硫主要的来源的是( )
| A、化石燃料的燃烧 |
| B、硫矿石的冶炼 |
| C、森林火灾 |
| D、硫酸、磷肥生产产生的废气 |
下列实验现象,与新制的氯水中的某些成分(括号内物质)没有关系的是( )
| A、氯水使红色布条褪色(HCl) |
| B、向NaHCO3固体中滴加氯水,有无色气泡(H+) |
| C、向氯水中滴加AgNO3溶液产生白色沉淀(Cl-) |
| D、向KI溶液中滴加氯水,再加淀粉溶液,溶液变蓝色(Cl2) |

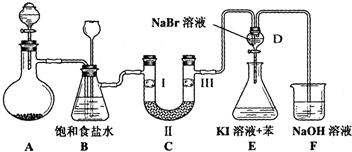
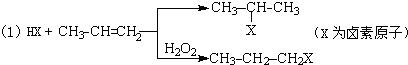
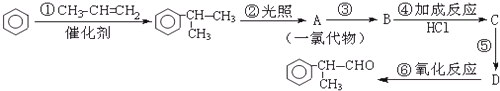
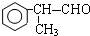 的物质,该物质是一种香料.
的物质,该物质是一种香料.