题目内容
5.下列化合物的核磁共振氢谱中出现两组峰且峰面积之比是2:1的是( )| A. | 乙酸甲酯 | B. | 对苯二酚 | C. | 2--甲基丙烷 | D. | 对二甲苯 |
分析 化合物的核磁共振氢谱中出现2组峰,说明有机物中含有2种类型的氢原子峰面积之比是2:1,氢原子数之比为2:1;分子中等效氢原子一般有如下情况:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效,以此来解答.
解答 解:A.乙酸甲酯结构简式为CH3COOCH3,两个甲基所处化学环境不同,故分子中有2种H原子,原子数目之比为3:3,故A不选;
B.对苯二酚( )中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为2:1,故B选;
)中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为2:1,故B选;
C.2-甲基丙烷的结构简式为CH3CH(CH3)CH3,中含有2种氢原子,核磁共振氢谱能出现两组峰,且其峰面积之比为9:1,故C不选;
D.对二甲苯的结构简式为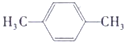 ,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,故D不选;
,该分子的核磁共振氢谱中有两组峰,其峰面积之比是3:2,故D不选;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握结构的对称性、核磁共振氢谱确定H的种类为解答的关键,侧重分析与应用能力的考查,注意H原子数目的判断,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
16.设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA | |
| B. | 8.8g乙酸乙酯中含共用电子对数为1.4 NA | |
| C. | 1 L 0.1 mol•L-1氯化铜溶液中铜离子数为0.1 NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
13.能够使醋酸溶液的c(H+)减小和醋酸的电离平衡逆向移动的条件是( )
| A. | 滴加少量H2SO4溶液 | B. | 加入少许水稀释 | ||
| C. | 滴加少量NaOH溶液 | D. | 加入少许CH3COONa晶体 |
20.下列叙述正确的是( )
| A. | 升高温度活化能降低 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 用电解水的方法制取大量氢气可以缓解能源不足的问题 | |
| D. | 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 |
10.把a、b、c、d四块金属片浸在稀硫酸中,用导线两两连接可以组成原电池,若a、b相连时b为负极;a、c相连时a极上产生大量气泡;b、d相连时b为正极;c、d相连时,电流由d到c.则这四种金属的活动性顺序由大到小为( )
| A. | a>c>b>d | B. | a>b>c>d | C. | c>d>b>a | D. | b>d>c>a |
17.下列表述正确的是( )
| A. | S2-的结构示意图: | B. | 碳原子电子式为 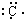 | ||
| C. | 氟化钠的电子式: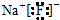 | D. | 氨气分子的结构式: |
14.实验室进行下列实验时,一定不需要使用“沸石”的是( )
| A. | 制取蒸馏水 | B. | 分馏石油 | C. | 制取乙烯 | D. | 溴乙烷的水解 |
1.下列各组物质中,既不是同系物,又不是同分异构体的是( )
| A. | 苯甲酸和 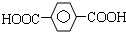 | B. | 乙酸和2-甲基丙酸 | ||
| C. | 硝基乙烷和氨基乙酸 | D. | 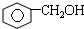 和 和 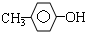 |