题目内容
石墨作电极电解氯化铜溶液,(如图),下列分析正确的是( )


| A、a端是直流电源的负极 |
| B、通电使氯化铜发生电离 |
| C、阳极上发生的反应:Cu2++2e→Cu |
| D、通电一段时间,在阴极附近观察到有黄绿色气体产生 |
考点:电解原理
专题:
分析:用石墨作电极电解氯化铜溶液,连接电源正极的为电解池的阳极,发生氧化反应:2Cl--2e-=Cl2↑,连接电源负极的为电解池的阴极,发生:Cu2++2e-=Cu,电解池工作时,阴离子向阳极移动,阳离子向阴极移动,以此解答该题.
解答:
解:A.铜离子向c端移动,说明c是电解池的阴极,则a端是直流电源的负极,故A正确;
B.氯化铜的电离只需溶于水,不需通电,故B错误;
C.阴极发生:Cu2++2e-=Cu,故C错误;
D.通电一段时间,在阳极发生氧化反应:2Cl--2e-=Cl2↑,阳极附近观察到有黄绿色气体产生,故D错误.
故选A.
B.氯化铜的电离只需溶于水,不需通电,故B错误;
C.阴极发生:Cu2++2e-=Cu,故C错误;
D.通电一段时间,在阳极发生氧化反应:2Cl--2e-=Cl2↑,阳极附近观察到有黄绿色气体产生,故D错误.
故选A.
点评:本题考查电解池知识,题目难度不大,注意把握电极的判断以及电极方程式的书写,为解答该题的关键.

练习册系列答案
相关题目
可逆反应mA(g)?n(B)+pC(s) )△H=QKJ?moL,温度和压强的变化对正、逆反应速率的影响分别符合图中的两个图象,以下叙述正确的是( )


| A、m>n,Q<0 |
| B、m>n+P.Q>0 |
| C、m>n,Q>0 |
| D、m<n+P,Q<0 |
在NaCl、MgCl2、MgSO4形成的混合溶液中,c(Na+)=0.2mol/L,c(Mg2+)=0.35mol/L,c(Cl-)=0.4mol/L,则c(SO42-)为( )
| A、0.10mol/L |
| B、0.15 mol/L |
| C、0.20 mol/L |
| D、0.25 mol/L |
下列物质的俗称、主要成分的化学式及其用途均正确的是( )
| A、磁铁矿--Fe2O3--炼铁 |
| B、胆矾--CuSO4?5H2O--波尔多液 |
| C、蓝宝石--SiO2--饰品 |
| D、纯碱--NaHCO3--焙制糕点 |
对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A、达到化学平衡时,5v正(O2)=4v逆(NO) |
| B、达到化学平衡时,3v正(NO)=2v正(H2O) |
| C、当NH3、O2、NO和H2O的浓度相等时,反应一定达到平衡状态 |
| D、达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大 |


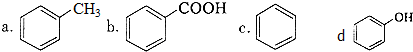
 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.
 .
. 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).

